题目内容
4.下列有关化学用语表示正确的是( )| A. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | B. | 水分子的比例模型: | ||
| C. | 硅的原子结构示意图: | D. | Na2S的电子式 |
分析 A.质量数=质子数+中子数,元素符号左上角为质量数、左下角为质子数;
B.水分子为V型,且 为球棍模型;
为球棍模型;
C.硅原子的核电荷数=核外电子总数=14,最外层含有4个电子;
D.硫化钠为离子化合物,电子式中需要标出所带电荷.
解答 解:A.中子数为20的氯原子的质量数为37,该原子正确的表示方法为:3717Cl,故A错误;
B.水分子为V型,氧原子的相对体积大于氢原子,其正确的比例模型为: ,故B错误;
,故B错误;
C.硅的原子核电荷数、核外电子总数都是14,其原子结构示意图为: ,故C正确;
,故C正确;
D.Na2S为离子化合物,钠离子用离子符号表示,硫离子标出最外层电子,硫化钠的电子式为 ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的表示方法,题目难度中等,涉及电子式、原子结构示意图、比例模型、元素符号等知识,明确常见化学用语的书写原则为解答关键,试题培养了学生的规范答题能力.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
12.如图所示的四个图象,能正确反映对应变化关系的是( )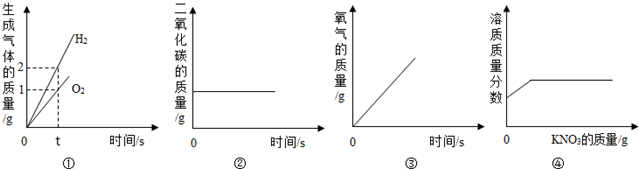

| A. | ①水的电解 | |
| B. | ②木炭在密闭的容器内燃烧 | |
| C. | ③加热一定量的高锰酸钾制氧气 | |
| D. | ④20℃时,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体 |
19.下列有关摩尔使用的说法中不正确的是( )
| A. | 1mol O | B. | 1mol O2 | C. | 1mol氧原子 | D. | 1摩尔小麦 |
9.铬铁矿的主要成分可表示为FeO•Cr2O3,还含有MgO、Al2O3、Fe2O3 等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图:
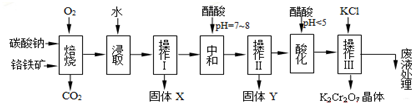
已知:①4FeO•Cr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3═2NaAlO2+CO2↑;
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)操作I的名称是过滤.
(2)下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl,该反应在溶液中能发生的理由是K2CrO7的溶解度比Na2Cr2O7小.
(3)操作Ⅲ有多步组成,获得K2Cr2O7晶体的操作依次是:加入KC1固体、蒸发浓缩、冷却结晶、过滤、洗涤、干燥.
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量NaOH溶液(填写试剂)、溶解、过滤、再通入足量CO2气体、…、灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26n}{17m}$×100%(用含m、n的代数式表示).
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL于碘量瓶中,加入10mL 2mol/L H2SO4和足量碘化钾,放于暗处5min.然后加入100mL水,加入3mL淀粉指示剂,用0.1000mol/LNa2S2O3标准溶液滴定.若实验中共用去Na2S2O3标准溶液47.40mL,则所得产品中重铬酸钾的纯度为92.9%.(保留3位有效数字)已知:①K2Cr2O7的摩尔质量为294g/mol
②Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
I2+2S2O32-═2I-+S4O62-.

已知:①4FeO•Cr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3═2NaAlO2+CO2↑;
③Cr2O72-+H2O?2CrO42-+2H+
根据题意回答下列问题:
(1)操作I的名称是过滤.
(2)下表是相关物质的溶解度数据,操作Ⅲ发生反应的化学方程式是:Na2Cr2O7+2KCl═K2Cr2O7↓+2NaCl,该反应在溶液中能发生的理由是K2CrO7的溶解度比Na2Cr2O7小.
| 物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
| 溶解度 (g/100g水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
| 40℃ | 40.1 | 36.4 | 26.3 | 215 | |
| 80℃ | 51.3 | 38 | 73 | 376 | |
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量NaOH溶液(填写试剂)、溶解、过滤、再通入足量CO2气体、…、灼烧、冷却、称量,得干燥固体m g.计算样品中氢氧化铝的质量分数为$\frac{26n}{17m}$×100%(用含m、n的代数式表示).
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL于碘量瓶中,加入10mL 2mol/L H2SO4和足量碘化钾,放于暗处5min.然后加入100mL水,加入3mL淀粉指示剂,用0.1000mol/LNa2S2O3标准溶液滴定.若实验中共用去Na2S2O3标准溶液47.40mL,则所得产品中重铬酸钾的纯度为92.9%.(保留3位有效数字)已知:①K2Cr2O7的摩尔质量为294g/mol
②Cr2O72-+6I-+14H+═2Cr3++3I2+7H2O;
I2+2S2O32-═2I-+S4O62-.
16.一定条件下,在密闭恒容容器中,能表示反应A(g)+2B(g)?2C(g)一定达到化学平衡状态的是( )
①A、B、C的物质的量之比为1:2:2
②A、B、C的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成nmolC,同时生成2nmolB
⑤v正(A)=v逆(C)
⑥混合气体的密度不再发生变化
⑦混合气体的平均相对分子质量不再发生变化.
①A、B、C的物质的量之比为1:2:2
②A、B、C的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成nmolC,同时生成2nmolB
⑤v正(A)=v逆(C)
⑥混合气体的密度不再发生变化
⑦混合气体的平均相对分子质量不再发生变化.
| A. | ①②⑦ | B. | ②④⑥ | C. | ②③⑦ | D. | ③④⑤ |
13.二氧化碳的回收利用是环保领域研究的热点课题.
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如图1所示.其总反应的化学方程式为CO2$\frac{\underline{\;△或太阳能\;}}{FeO}$C+O2.

(2)CO2经过催化氢化合成低碳烯烃.其合成乙烯的反应为2C02(g)+6H2(g)?CH2=CH2(g)+4H20(g)△H,
几种物质的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
则△H=-128kJ/mol
(3)在2L恒容密闭容器中充入2molCO2和nmol H2,在一定条件下发生(2)中的反应,CO2的转化率与温度、投料比[X=$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图2所示.
①X1> X2(填“>”、“<”或“=”,下同),平衡常数KA> KB.
②若B点的投料比为3,且从反应开始到B点需要10min,则v(H2)=0.225mol/(L.min).
(4)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如图3.
①b电极的名称是正极.
②产生丙烯的电极反应式为3CO2+18H++18e-=CH3CH=CH2+6H2O.
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如图1所示.其总反应的化学方程式为CO2$\frac{\underline{\;△或太阳能\;}}{FeO}$C+O2.

(2)CO2经过催化氢化合成低碳烯烃.其合成乙烯的反应为2C02(g)+6H2(g)?CH2=CH2(g)+4H20(g)△H,
几种物质的能量(在标准状况下,规定单质的能量为0,测得其他物质在生成时所放出或吸收的热量)如下表所示:
| 物质 | H2(g) | CO2(g) | CH2=CH2(g) | H2O(g) |
| 能量/kJ•mol-1 | 0 | -394 | 52 | -242 |
(3)在2L恒容密闭容器中充入2molCO2和nmol H2,在一定条件下发生(2)中的反应,CO2的转化率与温度、投料比[X=$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图2所示.
①X1> X2(填“>”、“<”或“=”,下同),平衡常数KA> KB.
②若B点的投料比为3,且从反应开始到B点需要10min,则v(H2)=0.225mol/(L.min).
(4)以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理图如图3.
①b电极的名称是正极.
②产生丙烯的电极反应式为3CO2+18H++18e-=CH3CH=CH2+6H2O.
14.下列说法正确的是( )
| A. | BaO2(过氧化钡)固体中的阴离子和阳离子之比为2:1 | |
| B. | 在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 | |
| C. | HCl的相对分子质量大于HF,所以HCl的沸点高于HF | |
| D. | 由ⅠA族和ⅥA族元素可形成原子个数比为1:1、电子总数为38的化合物 |
 .
.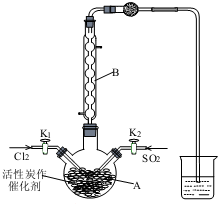 磺酰氯(SO2Cl2)用于有机合成、医药、染料、农药等,也用作表面活性剂,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.某学习小组用如图装置制备磺酰氯.(已知:SO2(g)+Cl2(g)?SO2Cl2(l)△H<0).
磺酰氯(SO2Cl2)用于有机合成、医药、染料、农药等,也用作表面活性剂,熔点-54.1℃,沸点69.1℃,遇水发生剧烈水解.某学习小组用如图装置制备磺酰氯.(已知:SO2(g)+Cl2(g)?SO2Cl2(l)△H<0).