题目内容
NA代表阿加德罗常数,下列说法正确的是( )
| A、氯化氢气体的摩尔质量等于NA个氯气分子和NA个氢气分子的质量之和 |
| B、常温常压下,1mol SO2约含有6.02×1023个SO2分子 |
| C、18g水中含有1mol H2和16g氧原子 |
| D、62g Na2O溶于水后所得溶液中含有O2-离子数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、摩尔质量的单位为g/mol,而质量的单位为g;
B、根据分子个数N=nNA来计算;
C、水分子由原子构成;
D、Na2O溶于水后和水反应生成NaOH,故所得溶液中无O2-离子.
B、根据分子个数N=nNA来计算;
C、水分子由原子构成;
D、Na2O溶于水后和水反应生成NaOH,故所得溶液中无O2-离子.
解答:
解:A、氯化氢气体的摩尔质量为36.5g/mol,NA个氯气分子和NA个氢气的物质的量都是1mol,质量之和为:71g+2g=73g,二者数值不同,单位也不同,故A错误;
B、1mol二氧化硫中的分子个数N=nNA=NA个,故B正确;
C、1个水分子由2个氢原子和1个氧原子构成,不含氢气,故C错误;
D、Na2O溶于水后和水反应生成NaOH,故所得溶液中无O2-离子,故D错误.
故选B.
B、1mol二氧化硫中的分子个数N=nNA=NA个,故B正确;
C、1个水分子由2个氢原子和1个氧原子构成,不含氢气,故C错误;
D、Na2O溶于水后和水反应生成NaOH,故所得溶液中无O2-离子,故D错误.
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
下列离子中最易给出电子的是( )
| A、Cl- |
| B、Cu2+ |
| C、Fe2+ |
| D、Al3+ |
在标准状况下,将22.4L HCl气体溶于水制成0.5L盐酸,所得盐酸的物质的量浓度为( )
| A、2mol/L |
| B、1.2mol/L |
| C、0.8mol/L |
| D、无法计算 |
设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、甲烷的摩尔质量与NA个甲烷分子的质量在数值上相等 |
| B、NA个氧气分子和NA个氢气分子的质量比等于16:1 |
| C、28 g氮气所含的原子数目为NA |
| D、17克NH3所含的原子数目为4NA,所含电子数目为10NA |
下列说法正确的是 ( )
| A、标况下,1mol任何物质的体积都约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、标况下,1molO2和N2混合气(任意比)的体积约为22.4L |
| D、22.4L气体所含分子数一定大于11.2L气体所含的分子数 |
下列各化合物的命名不正确的是( )
| A、CH2═CH-CH═CH2 1,4-二丁烯 |
B、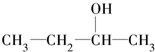 2-丁醇 2-丁醇 |
C、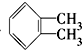 邻二甲苯 邻二甲苯 |
D、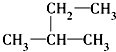 2-甲基丁烷 2-甲基丁烷 |
根据等电子原理,下列分子或离子与SO42-有相似结构的是( )
| A、PCl5 |
| B、CCl4 |
| C、NF3 |
| D、N |
