题目内容
下列各组离子能在某酸性的无色溶液中大量共存的是( )
| A、NH4+、Mg2+、SO42-、Cl- |
| B、Ca2+、I-、Na+、NO3- |
| C、Al3+、Cu2+、SO42-、Cl- |
| D、K+、Cl-、HCO3-、SO42- |
考点:离子共存问题
专题:离子反应专题
分析:强酸溶液中含大量的氢离子,根据离子之间不能结合生成沉淀、水、气体,不能发生氧化还原反应等,则离子大量共存,并结合离子的颜色来解答.
解答:
解:A.酸性溶液该组离子之间不反应,可大量共存,且离子均为无色,故A正确;
B.酸性溶液中I-、H+、NO3-发生氧化还原反应,不能大量共存,故B错误;
C.Cu2+为蓝色,与无色溶液不符,故C错误;
D.酸性溶液中H+、HCO3-结合生成水和气体,不能大量共存,故D错误;
故选A.
B.酸性溶液中I-、H+、NO3-发生氧化还原反应,不能大量共存,故B错误;
C.Cu2+为蓝色,与无色溶液不符,故C错误;
D.酸性溶液中H+、HCO3-结合生成水和气体,不能大量共存,故D错误;
故选A.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
物质间常常相互联系、互相影响着,微粒也不例外.下列各组离子可能大量共存的是( )
| A、不能使酚酞试液变红的无色溶液中:Na+、CO32-、K+、C1O-、I- |
| B、能与金属铝反应放出氢气的溶液中:K+、NO3-、C1-、NH4+ |
| C、常温下水电离出的c(H+)?c(OH-)=10-20的溶液中:Na+、Cl-、S2-、SO32- |
| D、无色透明溶液:K+、HCO3-、NO3-、SO42-、Fe3+ |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、7.8 g Na2O2含有的阴离子数目为0.2 NA |
| B、PH=2的醋酸冲稀10倍后,溶液中H+数目大于0.001NA |
| C、1 mol FeCl3跟水完全反应转化为氢氧化铁胶体后,胶体粒子的数目小于NA |
| D、1.8 g重水(D2O)中含NA个质子和NA个中子 |
以下说法不正确的是( )
| A、绿色食品是指不含任何化学物质的食品 |
| B、硅是制造太阳能电池的常用材料 |
| C、SiO2、SO2均属酸性氧化物 |
| D、光导纤维是以二氧化硅为主要原料制成的 |
下列各组离子,能在溶液中大量共存的是( )
| A、Na+、Cu2+、Cl-、SO42- |
| B、Na+、Ca2+、CO32-、NO3- |
| C、Na+、H+、Cl-、CO32- |
| D、K+、H+、SO42-、OH- |
下列物质长久放置在空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A、浓硫酸的质量增加 |
| B、铝的表面生成致密的氧化物薄膜 |
| C、澄清的石灰水变浑浊 |
| D、氢氧化钠固体发生潮解 |
已知氧化还原反应:KClO3+6HCl═3Cl2↑+KCl+3H2O,下列说法正确的是( )
| A、Cl2是氧化产物,KCl是还原产物 |
| B、盐酸在该反应中只表现还原性 |
| C、每生成3 mol Cl2,有1 mol KClO3发生氧化反应 |
| D、每转移0.1 mol电子,能生成标准状况1344mLCl2 |
如图所示的装置或操作正确的是( )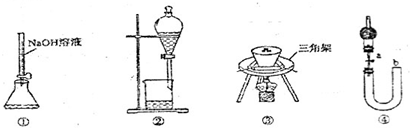

| A、用装置①量取15.00mL的NaOH溶液 |
| B、用装置②分离苯和水的混合物,苯应从下口流出 |
| C、用装置③陶瓷坩埚高温煅烧CaCO3固体 |
| D、关闭活塞a,从b处加水,以检查装置④的气密性 |