题目内容
下列物质长久放置在空气中会发生相应的变化,其中发生了氧化还原反应的是( )
| A、浓硫酸的质量增加 |
| B、铝的表面生成致密的氧化物薄膜 |
| C、澄清的石灰水变浑浊 |
| D、氢氧化钠固体发生潮解 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:判断元素的化合价是否发生改变,如发生改变,则发生氧化还原反应.
解答:
解:A.浓硫酸具有吸水性而增重,属于物理变化,故A错误;
B.铝表面生成致密的薄膜,是由于Al被空气中氧气氧化为氧化铝的原因,发生氧化还原反应,故B正确;
C.澄清的石灰水与空气中二氧化碳反应生成碳酸钙而变浑浊,发生复分解反应,故C错误;
D.氢氧化钠固体发生潮解,是氢氧化钠吸收了空气中的水蒸气,属于物理变化,故D错误.
故选B.
B.铝表面生成致密的薄膜,是由于Al被空气中氧气氧化为氧化铝的原因,发生氧化还原反应,故B正确;
C.澄清的石灰水与空气中二氧化碳反应生成碳酸钙而变浑浊,发生复分解反应,故C错误;
D.氢氧化钠固体发生潮解,是氢氧化钠吸收了空气中的水蒸气,属于物理变化,故D错误.
故选B.
点评:本题考查氧化还原反应,题目难度不大,注意物质的性质,从化合价变化的角度分析氧化还原反应.

练习册系列答案
相关题目
下列溶液中微粒的浓度关于不正确的是( )
| A、NaClO溶液中:c(Na+)=c(HClO)+c(ClO-) |
| B、等体积、等物质的量浓度的NaX和弱酸HX混合,所得溶液中:c(Na+)>c(X-)>c(H+)>c(OH-) |
| C、将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(NH4+)>c(Cl-)>c(NH3?H2O)>c(OH-)>c(H+) |
| D、将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-) |
下列过程表达式中,属于电离方程式的是( )
| A、NH3+H+=NH4+ |
| B、HCO3-+OH-=H2O+CO32- |
| C、HCO3-+H2O?H2CO3+OH- |
| D、NH3?H2O?NH4++OH- |
下列各组离子能在某酸性的无色溶液中大量共存的是( )
| A、NH4+、Mg2+、SO42-、Cl- |
| B、Ca2+、I-、Na+、NO3- |
| C、Al3+、Cu2+、SO42-、Cl- |
| D、K+、Cl-、HCO3-、SO42- |
砷是氮族元素,黄砷(As4)是其一种单质,其分子结构与白磷(P4)相似,以下关于黄砷与白磷的比较叙述正确的是( )
| A、分子中共价键键角均为60° |
| B、黄砷中共价键键能大于白磷 |
| C、分子中含有的共价键的数目都是4 |
| D、黄砷的熔点低于白磷 |
提纯含有少量Ba(NO3)2杂质的KNO3溶液,可以使用的方法是( )
| A、加入过量的K2CO3溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
| B、加入过量的K2SO4溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
| C、加入过量的Na2CO3溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
| D、加入过量的Na2SO4溶液,过滤,除去沉淀,滤液中补加适量硝酸 |
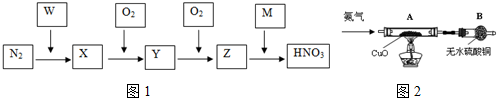
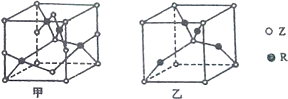 已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题:
已知元素W、X、Y、Z、R为前四周期元素,且原子序数依次增大.元素W的负一价阴离子与某惰性气体结构相同,X是形成化合物种类最多的元素,Z原子L电子层上有2对成对电子,R+原子核外有3层电子且各层均处于全满状态.请回答下列问题: