题目内容
12.下列说法正确的是( )| A. | 按照系统命名法,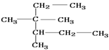 的名称为2,3-二甲基-2-乙基戊烷 的名称为2,3-二甲基-2-乙基戊烷 | |
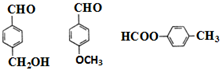
| B. | 除去苯中 的方法:加溴水,充分振荡,静置分液 的方法:加溴水,充分振荡,静置分液 | |
| C. | 1mol 最多能与4mol氢氧化钠反应 最多能与4mol氢氧化钠反应 | |
| D. | 苯乙烯中所有原子不可能共平面 |
分析 A.主链含6个C,3、4号C上有甲基;
B. 与溴水发生加成反应的产物及溴均易溶于苯;
与溴水发生加成反应的产物及溴均易溶于苯;
C.酚-OH、-COOC-及水解生成的酚-OH均与NaOH反应;
D.苯环及碳碳双键均为平面结构,且直接相连.
解答 解:A.主链含6个C,3、4号C上有甲基,则名称为3,3,4-三甲基-己烷,故A错误;
B. 与溴水发生加成反应的产物及溴均易溶于苯,不能除杂,应选蒸馏法,故B错误;
与溴水发生加成反应的产物及溴均易溶于苯,不能除杂,应选蒸馏法,故B错误;
C.酚-OH、-COOC-及水解生成的酚-OH均与NaOH反应,则1mol 最多能与4mol氢氧化钠反应,故C正确;
最多能与4mol氢氧化钠反应,故C正确;
D.苯环及碳碳双键均为平面结构,且直接相连,则苯乙烯中所有原子能共平面,故D错误;
故选C.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的性质、原子共面、命名等为解答的关键,侧重分析与应用能力的考查,选项C为解答的易错点,题目难度不大.

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
5.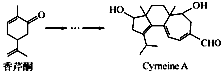 Cyrneine A对治疗神经系统疾病有着很好的疗效.可用香芹酮经过多步反应合成:下列说法不正确的是( )
Cyrneine A对治疗神经系统疾病有着很好的疗效.可用香芹酮经过多步反应合成:下列说法不正确的是( )
 Cyrneine A对治疗神经系统疾病有着很好的疗效.可用香芹酮经过多步反应合成:下列说法不正确的是( )
Cyrneine A对治疗神经系统疾病有着很好的疗效.可用香芹酮经过多步反应合成:下列说法不正确的是( )| A. | 香芹酮的分子式为C10H14O | |
| B. | Cyrneine A可以发生加成反应、消去反应和氧化反应 | |
| C. | 香芹酮和Cyrneine A均能使酸性KMnO4溶液褪色 | |
| D. | 与香芹酮互为同分异构体,分子中有4种不同化学环境的氢原子的酚类化合物共有3种 |
20.下列关于物质的用途或变化的说法正确的是( )
| A. | 耐火陶瓷可以选用熔点很高的 Al2O3等材料制作 | |
| B. | 含量为 99.9999%的高纯硅用于制作光导纤维 | |
| C. | 高炉炼铁可用铝热反应来迚行冶炼 | |
| D. | “雷雨肥田“是因为 N2不O2在放电条件下生成氮的化合物 |
17.下列说法正确的是 ( )
| A. | 工业上冶炼活泼金属的单质都是通过电解法 | |
| B. | 工业上冶炼粗硅是用热还原法 | |
| C. | 消耗等质量的氢气,碱性氢氧电池放电量大于酸性介质的放电量 | |
| D. | 硫酸工业的尾气可以用氨水吸收并制得铵盐 |
4.已知:2R-Cl+2Na→R-R+2NaCl(R代表烃基),下列有机物通过上述反应可制得对二甲基环己烷的是
( )
( )
| A. | 2,3-二氯丁烷 | B. | 1,3-二氯丁烷 | ||
| C. | 2-氯丁烷 | D. | 2,5-二氯己烷和1,2-二氯乙烷 |
16.下列离子方程式正确的是( )
| A. | 向苯酚钠溶液中通入少量的SO2气体:C6H5O-+SO2+H2O→C6H5OH+HSO3- | |
| B. | 次氯酸钙溶液中通入过量二氧化碳:ClO-+H2O+CO2═HCO3-+HClO | |
| C. | 向NaHSO4溶液中滴加Ba(OH)2至溶液恰好呈现中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 用惰性电极电解MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ |
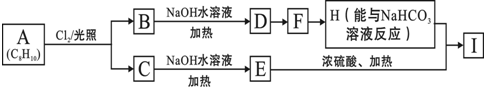
 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2 +2H2O.
+2H2O.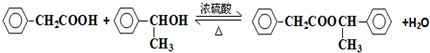 .
. .
.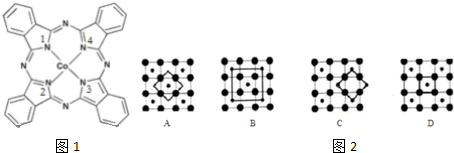
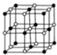 ),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述 CoO2的化学组成的是D.
),在该晶体中与一个钴原子等距离且最近的钴原子有12个;筑波材料科学国家实验室一个科研小组发现了在5K下呈现超导性的晶体,该晶体具有CoO2的层状结构(如图2所示,小球表示Co原子,大球表示O原子).下列用粗线画出的重复结构单元示意图不能描述 CoO2的化学组成的是D.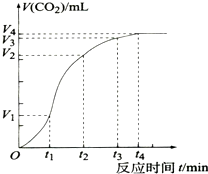 为了研究CaCO3与稀盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制曲线(图),已知该反应是放热反应,请分析讨论以下问题:
为了研究CaCO3与稀盐酸反应的反应速率,某同学通过实验测定反应中生成的CO2气体体积随反应时间变化的情况,绘制曲线(图),已知该反应是放热反应,请分析讨论以下问题: