题目内容
常温 下,0.1mol/L氨水中
=1×10-10,下列说法正确的是( )
| c(H+) |
| c(OH-) |
| A、溶液中由水电离出的c(OH-)=1×10-10mol/L |
| B、溶液中c(OH-)+c(NH3?H2O)=0.1mol/L |
| C、与0.1mol/L 的盐酸等体积混合后所得溶液中:c(Cl-)=c(NH4+)+c(NH3?H2O)=0.1mol/L |
| D、原溶液中加入少量的氯化铵晶体或加水稀释,溶液中的c(H+)均增大 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:A、根据常温下,0.1mol/L氨水中
=1×10-10,则溶液中c(H+)=1×10-12mol/L,c(OH-)=1×10-2mol/L,所以由水电离的c(OH-)=1×10-12mol/L;
B、根据物料守恒及其离子浓度大小判断;
C、与0.1mol/L 的盐酸等体积混合后所得溶液体积增大一倍,所以浓度应该变成原来的
;
D、在原溶液中加氯化铵晶体,氨水的电离平衡逆向移动,碱性减弱,c(H+)增大,在原溶液中加水稀释,虽然电离平衡向正向移动但是碱性减弱,c(H+)增大.
| c(H+) |
| c(OH-) |
B、根据物料守恒及其离子浓度大小判断;
C、与0.1mol/L 的盐酸等体积混合后所得溶液体积增大一倍,所以浓度应该变成原来的
| 1 |
| 2 |
D、在原溶液中加氯化铵晶体,氨水的电离平衡逆向移动,碱性减弱,c(H+)增大,在原溶液中加水稀释,虽然电离平衡向正向移动但是碱性减弱,c(H+)增大.
解答:
解:A、根据常温下,0.1mol/L氨水中
=1×10-10,则溶液中c(H+)=1×10-12mol/L,c(OH-)=1×10-2mol/L,所以由水电离的c(OH-)=1×10-12mol/L,故A错误;
B、根据物料守恒,则c(NH4+)+c(NH3?H2O)=0.1mol/L,又溶液中c(NH4+)<c(OH-),所以c(OH-)+c(NH3?H2O)>0.1mol/L,故B错误;
C、与0.1mol/L 的盐酸等体积混合后所得溶液体积增大一倍,所以浓度应该变成原来的
,所以c(Cl-)=c(NH4+)+c(NH3?H2O)=0.05mol/L,故C错误;
D、在原溶液中加氯化铵晶体,氨水的电离平衡逆向移动,碱性减弱,c(H+)增大,在原溶液中加水稀释,虽然电离平衡向正向移动但是碱性减弱,c(H+)增大,故D正确;
故选:D.
| c(H+) |
| c(OH-) |
B、根据物料守恒,则c(NH4+)+c(NH3?H2O)=0.1mol/L,又溶液中c(NH4+)<c(OH-),所以c(OH-)+c(NH3?H2O)>0.1mol/L,故B错误;
C、与0.1mol/L 的盐酸等体积混合后所得溶液体积增大一倍,所以浓度应该变成原来的
| 1 |
| 2 |
D、在原溶液中加氯化铵晶体,氨水的电离平衡逆向移动,碱性减弱,c(H+)增大,在原溶液中加水稀释,虽然电离平衡向正向移动但是碱性减弱,c(H+)增大,故D正确;
故选:D.
点评:本题考查了弱电解质的电离、酸碱混合溶液定性判断等知识点,根据酸碱混合溶液的酸碱性结合电荷守恒来分析解答,易错选项是A,注意:碱中氢氧根离子浓度不等于由水电离出的氢氧根离子浓度,为易错点.

练习册系列答案
相关题目
常温熔融盐又称常温离子液体(ionic liquid),1914年报道的第一种离子液体硝酸乙基铵〔(C2H5NH3)NO3〕,其熔点为12℃.已知C2H5NH2结合质子的能力比NH3略强,下列有关硝酸乙基铵的说法正确的是( )
| A、该离子液体中含氨分子 |
| B、硝酸乙基铵水溶液呈碱性 |
| C、硝酸乙基铵水解的离子方程式可表示为:C2H5NH3++2H2O?C2H5NH2?H2O+H3O+ |
| D、同温度下相同物质的量浓度的硝酸乙基铵溶液和硝酸铵溶液前者的pH小 |
铝土矿的主要成分为氧化铝,还有少量的氧化铁和二氧化硅杂质.工业上经过下列工艺可以冶炼金属铝:下列说法中正确的是( )


| A、滤液A可用于净水,其净水原理为Al3++3H2O═Al(OH)3+3H+ |
| B、固体C→固体D的操作过程中主要仪器是酒精灯、蒸馏皿、玻璃棒 |
| C、滤液C中存在以下关系:c(Na+)=c(SO42-)+2 c(CO32-)+c(HCO3-)+c(OH-)-c(H+) |
| D、若在100 mL滤液B中加入1 mol?L-1HCl 200 mL,沉淀达到最大且质量为11.7 g,则滤液B中c(Na+)大小2 mol?L |
有4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成:①CH3COONa与HCl;②CH3COONa与NaOH;③CH3COONa与NaCl;④CH3COONa与NaClO 下列各项排序正确的是( )
| A、pH:②>③>④>① |
| B、c(CH3COO-):②>④>③>① |
| C、溶液中c(H+):①>③>②>④ |
| D、c(CH3COOH):①>④>③>② |
下列物质跟铁发生反应能生成三价铁盐的是( )
| A、稀硫酸 | B、硫酸铜 |
| C、硫磺 | D、氯气 |
实验室制取氧气的反应为2KMnO4
K2MnO4+MnO2+3O2↑,反应后从剩余物中回收二氧化锰的操作顺序正确的是( )
| ||
| A、溶解、过滤、洗涤、干燥 |
| B、溶解、过滤、蒸发、洗涤 |
| C、溶解、蒸发、洗涤、过滤 |
| D、溶解、洗涤、过滤、加热 |
下列试剂不会因为空气中的氧气而变质的是( )
| A、亚硫酸钠 | B、漂白粉 |
| C、硫酸亚铁 | D、氢硫酸 |
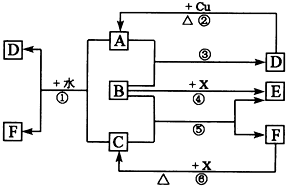 下列各物质为中学化学中常见物质,其中A、C、E、F为气体,B、D为无色液体,D是一种重要的化工原料,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,A是形成酸雨的主要气体.反应中部分生成物已略去.
下列各物质为中学化学中常见物质,其中A、C、E、F为气体,B、D为无色液体,D是一种重要的化工原料,F的浓溶液与X共热通常用于实验室制备单质C,X是一种黑色粉末,B分子中有18个电子,A是形成酸雨的主要气体.反应中部分生成物已略去.