题目内容
【题目】下列叙述中,正确的是 ( )
A. H2SO4的摩尔质量是98
B. 等质量的CO与CO2中所含碳原子数之比为7︰11
C. 等质量的O2和O3中所含的氧原子数相同
D. 98g H2SO4溶解于500mL 所得溶液中硫酸的物质的量浓度为2 molL-1
【答案】C
【解析】
A.H2SO4的摩尔质量是98g/mol;B.根据n=![]() 计算判断物质的量关系,再根据分子中含有的C原子数目判断; C.O2和O3都由氧原子构成,二者质量相等含有的氧原子数目相等;D.98g H2SO4的物质的量为1mol,溶于水配成500mL溶液,所得溶液中硫酸的物质的量浓度为2 mol/L。
计算判断物质的量关系,再根据分子中含有的C原子数目判断; C.O2和O3都由氧原子构成,二者质量相等含有的氧原子数目相等;D.98g H2SO4的物质的量为1mol,溶于水配成500mL溶液,所得溶液中硫酸的物质的量浓度为2 mol/L。
A.H2SO4的摩尔质量是98g/mol,1molH2SO4的质量是98g,选项A错误;B.等质量的CO与CO2的物质的量之比为![]() :
:![]() =11:7,二者分子都含有1个C原子,二者所含碳原子数之比为11:7,选项B错误;C. O2和O3都由氧原子构成,二者质量相等含有的氧原子数目相等,选项C正确;D.98g H2SO4的物质的量为1mol,溶于水配成500mL溶液,所得溶液中硫酸的物质的量浓度为2 mol/L,体积500mL是指溶液的体积,不是溶剂的体积,选项D错误;答案选C。
=11:7,二者分子都含有1个C原子,二者所含碳原子数之比为11:7,选项B错误;C. O2和O3都由氧原子构成,二者质量相等含有的氧原子数目相等,选项C正确;D.98g H2SO4的物质的量为1mol,溶于水配成500mL溶液,所得溶液中硫酸的物质的量浓度为2 mol/L,体积500mL是指溶液的体积,不是溶剂的体积,选项D错误;答案选C。

【题目】水溶性离子是大气颗粒物的主要成分,研究其化学组成对于治理大气污染其有重大意义,某地区大气颗粒物经采样与必要的预处理后得试样溶液。经离子色谱检验确定含有以下离子NH4+、Na+、Mg2+、Ca2+、Al3+、SO42-、NO3-、CO32-、Cl-。某同学对其再进行如下的实验:
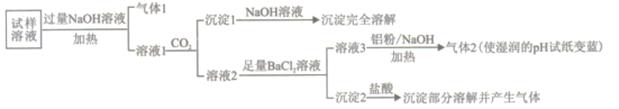
已知:在加热与强碱性条件下,铝单质可以将NO3-还原为氨气。
回答下列问题:
(1)“气体1“的电子式为_________。
(2)生成“沉淀1”的离子方程式为________。
(3)“沉定2”的成分是___________(填化学式)。
(4)“溶液3![]() 气体2”的离子方程式为_________。
气体2”的离子方程式为_________。
(5)根据上述实验可推断该地区大气颗粒物中__________含量较低(填离子符号)。
(6)已知大气颗粒物中各元素的行染主体如下表:
元素 | N | S | Na、Mg、Cl | Al | Ca |
污染主体 | 机动车尾气 | 燃煤污染 | 海盐离子 | 土壤扬尘 | 建筑粉尘 |
根据实验结果可判断该地区大气颗粒物污染主体有___________。