题目内容
过氧化钠与足量的碳酸氢钠固体混合后,在密闭容器中充分加热,排出气体物质后冷却,残留的固体物质是( )
| A、Na2O2、Na2CO3 |
| B、Na2CO3 |
| C、Na2CO3、NaOH |
| D、Na2O2、Na2CO3、NaOH |
考点:有关混合物反应的计算,化学方程式的有关计算
专题:
分析:加热时碳酸氢钠分解生成二氧化碳和水,分别与过氧化钠反应生成碳酸钠和氢氧化钠,当碳酸氢钠过量时,生成二氧化碳过量,又与氢氧化钠反应生成碳酸钠,最终产物为碳酸钠.
解答:
解:NaHCO3加热分解:2NaHCO3
Na2CO3+CO2↑+H2O,
生成的CO2和H2O分别与Na2O2反应:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
由于NaHCO3足量,则会发生:CO2+2NaOH=Na2CO3+H2O,
所以残留固体为Na2CO3,
故选B.
| ||
生成的CO2和H2O分别与Na2O2反应:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2↑,
由于NaHCO3足量,则会发生:CO2+2NaOH=Na2CO3+H2O,
所以残留固体为Na2CO3,
故选B.
点评:本题考查钠的化合物的性质,难度不大,注意NaHCO3足量的特点,根据发生的有关反应正确判断最终产物.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
一定量的镁铝合金与足量的氢氧化钠溶液反应产生3.36L氢气.若将等质量的该合金完全溶于稀硝酸,反应中硝酸被还原只产生4.48L的NO(气体的体积均已折算到标准状况),在反应后的溶液中,加入足量的氢氧化钠溶液,生成沉淀的质量为( )
| A、11.4g | B、16.5g |
| C、9.7g | D、8.7g |
下列有机化合物的分类不正确的是( )
A、 苯的同系物 苯的同系物 |
B、 芳香族化合物 芳香族化合物 |
C、 不饱和烃 不饱和烃 |
D、 醇 醇 |
下列反应中,改变反应物的用量或浓度,不会改变生成物的是( )
| A、碳粉和氧气反应 |
| B、细铁丝在氧气中燃烧 |
| C、二氧化碳通入氢氧化钠溶液中 |
| D、铜和硝酸反应 |
某同学搜集资料发现,长期或大量摄入铝元素会对人的大脑和神经系统造成损害,为此该同学提出的下列建议中错误的是( )
| A、少吃油条,因为油条中含有KAl(SO4)2 |
| B、使用铝锅时,应加醋长时间炖煮 |
| C、使用铁锅代替铝制炊具 |
| D、治疗胃酸过多时尽量不服用含Al(OH)3的胃药 |
下列物质性质与应用对应关系正确的是( )
| A、氨气具有碱性,可用作制冷剂 |
| B、二氧化硅能与氢氟酸反应,可用于生产光导纤维 |
| C、铝具有良好导电性和耐腐蚀性,可用于制作高压输电线 |
| D、二氧化铅具有强氧化性,可用于铅蓄电池的负极材料 |
下列图示与对应的叙述相符的是( )
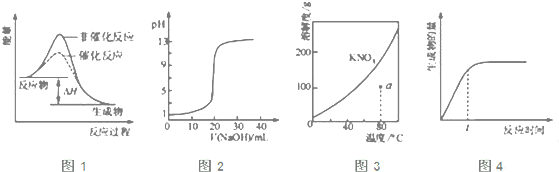

| A、图1表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
| B、图2表示0.1000 mol?L-1NaOH溶液滴定20.00mL0.1000 mol?L-1CH3COOH溶液所得到的滴定曲线 |
| C、图3表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液 |
| D、图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v正<v逆 |