题目内容
2010年诺贝尔化学奖获得者赫克、伊智根岸(美)和铃木彰(日)在钯催化交叉偶联反应方面的研究,为化学家提供了更为精确、有效的工具,极大促进了制造复杂化学物质的可能性.已知一种钯催化的交叉偶联反应可以表示为:
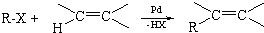
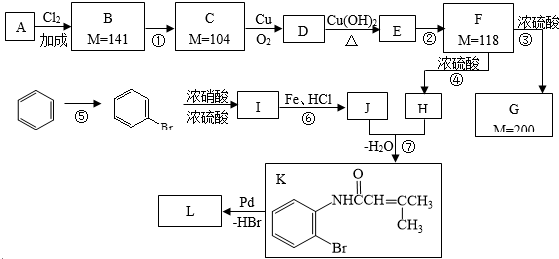
下面是利用钯催化的交叉偶联反应,以烃A与苯为原料合成某个复杂分子L(相对质量不超过200)的过程,其中F在浓硫酸作用下可以发生两种不同的反应分别形成H和G.
(1)写出反应的反应类型:④ ⑥
(2)写出反应需要的无机反应物、反应条件:
① ,⑤ ;
(3)根据要求完成下列两个空格:
用系统命名法给物质A命名: ;
写出物质L的结构简式: .
(4)写出下列反应的化学方程式:
C→D: ;
F→G: .
(5)H有多种同分异构体,请写出一种符合下列条件的结构简式: .
i.能发生水解反应 ii.分子中只含有两个甲基 iii.不含环状结构.
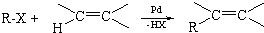
下面是利用钯催化的交叉偶联反应,以烃A与苯为原料合成某个复杂分子L(相对质量不超过200)的过程,其中F在浓硫酸作用下可以发生两种不同的反应分别形成H和G.

(1)写出反应的反应类型:④
(2)写出反应需要的无机反应物、反应条件:
①
(3)根据要求完成下列两个空格:
用系统命名法给物质A命名:
写出物质L的结构简式:
(4)写出下列反应的化学方程式:
C→D:
F→G:
(5)H有多种同分异构体,请写出一种符合下列条件的结构简式:
i.能发生水解反应 ii.分子中只含有两个甲基 iii.不含环状结构.
考点:有机物的合成
专题:有机物的化学性质及推断
分析:根据K的结构为邻位,则溴苯发生消化反应生成I为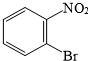 ,I在铁、氯化氢条件下发生还原反应生成J为
,I在铁、氯化氢条件下发生还原反应生成J为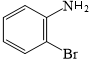 ,J与H发生脱水生成K,则根据K的结构可推知H为
,J与H发生脱水生成K,则根据K的结构可推知H为 ,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为
,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为 ,G为
,G为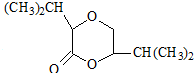 ;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为
;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为 ,D为
,D为 ,E为
,E为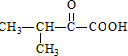 ,B为
,B为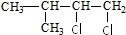 ,A为
,A为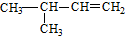 ,据此分析解答;
,据此分析解答;
 ,I在铁、氯化氢条件下发生还原反应生成J为
,I在铁、氯化氢条件下发生还原反应生成J为 ,J与H发生脱水生成K,则根据K的结构可推知H为
,J与H发生脱水生成K,则根据K的结构可推知H为 ,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为
,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为 ,G为
,G为 ;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为
;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为 ,D为
,D为 ,E为
,E为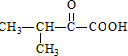 ,B为
,B为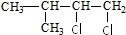 ,A为
,A为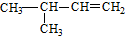 ,据此分析解答;
,据此分析解答;解答:
解:根据K的结构为邻位,则溴苯发生消化反应生成I为 ,I在铁、氯化氢条件下发生还原反应生成J为
,I在铁、氯化氢条件下发生还原反应生成J为 ,J与H发生脱水生成K,则根据K的结构可推知H为
,J与H发生脱水生成K,则根据K的结构可推知H为 ,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为
,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为 ,G为
,G为 ;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为
;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为 ,D为
,D为 ,E为
,E为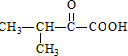 ,B为
,B为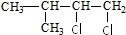 ,A为
,A为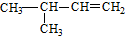 ;
;
(1)根据以上分析,反应④为F在浓硫酸作用下发生消去反应生成H,反应⑥为I在铁、氯化氢条件下发生还原反应生成J,故答案为:消去反应;还原反应;
(2)根据以上分析,反应①为B在氢氧化钠溶液加热条件下发生水解反应生成C,反应⑤为苯在液溴,铁粉作催化剂条件下发生取代反应生成溴苯,故答案为:NaOH水溶液,加热;液溴,铁粉;
(3)根据以上分析,A为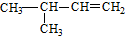 ,名称为3-甲基-1-丁烯;根据流程K发生信息反应生成L,则L为
,名称为3-甲基-1-丁烯;根据流程K发生信息反应生成L,则L为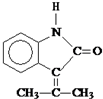 ,故答案为:3-甲基-1-丁烯;
,故答案为:3-甲基-1-丁烯; ;
;
(4)根据以上分析,C到D的反应为: ;
;
F→G为: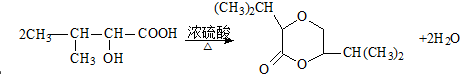 ,故答案为:
,故答案为: ;
; ;
;
(5)H为 ,有多种同分异构体i.能发生水解反应,说明含有酯基;ii.分子中只含有两个甲基iii.不含环状结构,所以符合条件的结构简式为:
,有多种同分异构体i.能发生水解反应,说明含有酯基;ii.分子中只含有两个甲基iii.不含环状结构,所以符合条件的结构简式为: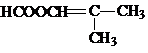 ,故答案为:
,故答案为: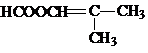 ;
;
 ,I在铁、氯化氢条件下发生还原反应生成J为
,I在铁、氯化氢条件下发生还原反应生成J为 ,J与H发生脱水生成K,则根据K的结构可推知H为
,J与H发生脱水生成K,则根据K的结构可推知H为 ,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为
,因为F在浓硫酸作用下可以发生两种不同的反应分别形成H和G,又由H的相对分子质量为100,F为118,G为200,则F在浓硫酸作用下发生消去反应生成H,2分子F在浓硫酸作用下脱去2分子水发生分子间酯化反应生成G,则F为 ,G为
,G为 ;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为
;烃A与氯气发生加成反应生成B,根据B的相对分子质量141,则烃A的相对分子质量70,分子式为C5H10,B含有2个氯原子,又B(141)发生反应①生成C(104),由相对分子质量得出B在氢氧化钠溶液中发生水解反应生成C,则C中含有2个羟基,又C催化氧化生成D,D与新制的氢氧化铜反应生成E,E又反应生成F,根据F的结构简式,则C为 ,D为
,D为 ,E为
,E为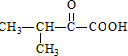 ,B为
,B为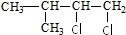 ,A为
,A为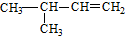 ;
;(1)根据以上分析,反应④为F在浓硫酸作用下发生消去反应生成H,反应⑥为I在铁、氯化氢条件下发生还原反应生成J,故答案为:消去反应;还原反应;
(2)根据以上分析,反应①为B在氢氧化钠溶液加热条件下发生水解反应生成C,反应⑤为苯在液溴,铁粉作催化剂条件下发生取代反应生成溴苯,故答案为:NaOH水溶液,加热;液溴,铁粉;
(3)根据以上分析,A为
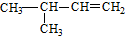 ,名称为3-甲基-1-丁烯;根据流程K发生信息反应生成L,则L为
,名称为3-甲基-1-丁烯;根据流程K发生信息反应生成L,则L为 ,故答案为:3-甲基-1-丁烯;
,故答案为:3-甲基-1-丁烯; ;
;(4)根据以上分析,C到D的反应为:
 ;
;F→G为:
 ,故答案为:
,故答案为: ;
; ;
;(5)H为
 ,有多种同分异构体i.能发生水解反应,说明含有酯基;ii.分子中只含有两个甲基iii.不含环状结构,所以符合条件的结构简式为:
,有多种同分异构体i.能发生水解反应,说明含有酯基;ii.分子中只含有两个甲基iii.不含环状结构,所以符合条件的结构简式为: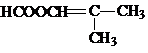 ,故答案为:
,故答案为: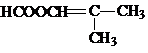 ;
;
点评:本题考查有机物的推断,题目难度较大,本题注意采用逆推法,为解答该题的关键,注意有机物官能团的性质和相对分子质量的利用,较好的考查学生的自学能力、逻辑推理能力,是热点题型.

练习册系列答案
相关题目
将3.64gFe2O3和Al2O3样品溶解在过量的200mLpH=1的盐酸溶液中,然后向其中加入NaOH溶液使Fe3+、Al3+刚好完全沉淀,用去NaOH溶液100mL,则NaOH溶液的浓度为( )
| A、0.1mol/L |
| B、0.2mol/L |
| C、0.4mol/L |
| D、0.8mol/L |
下列除去杂质的方法不正确的是( )
| A、镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B、用过量氨水除去Fe3+溶液中的少量Al3+ |
| C、Al(OH)3中混有少量Mg(OH)2:加入过量烧碱溶液充分反应,过滤,向滤液中通入过量CO2后过滤 |
| D、可以用过量氢氧化钠溶液除去MgO中的少量Al2O3 |
过氧化钠与足量的碳酸氢钠固体混合后,在密闭容器中充分加热,排出气体物质后冷却,残留的固体物质是( )
| A、Na2O2、Na2CO3 |
| B、Na2CO3 |
| C、Na2CO3、NaOH |
| D、Na2O2、Na2CO3、NaOH |
对于反应I2(g)+H2(g)?2HI(g),在其他条件不变的情况下能增大正反应速率的措施是( )
| A、移走部分HI |
| B、减小容器容积 |
| C、通入大量氦气 |
| D、降低体系温度 |
化学与生活密切相关,下列说法不正确的是( )
| A、“酸雨”、“臭氧层受损”、“光化学烟雾”都与氮氧化物有关 |
| B、PM2.5作为空气质量预报的一项重要指标,它是指空气中直径小于或等于2.5μm的颗粒物,该值越高,代表空气污染程度越严重 |
| C、静电除尘治理悬浮颗粒污染,其依据是胶体的电泳原理 |
| D、为消除碘缺乏症,卫生部规定食盐中必须加含碘物质.食盐中所加含碘物质是KI |
 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2CO3溶液将这三种离子逐一沉淀分离.其流程图如图所示
某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2CO3溶液将这三种离子逐一沉淀分离.其流程图如图所示