题目内容
4.下列说法正确的是( )| A. | 氧化还原反应中,一定有一种元素被氧化,另一种元素被还原 | |
| B. | 物质所含元素的化合价越高,该物质的氧化性就越强 | |
| C. | HClO既有氧化性,又有还原性 | |
| D. | 1molCl2参加反应转移2mol电子 |
分析 A.可能只有一种元素的化合价变化;
B.稀硫酸中S为最高价,不具有强氧化性;
C.HClO可分解生成HCl和氧气;
D.氯气与水反应生成HCl、HClO.
解答 解:A.可能只有一种元素的化合价变化,如氯气与水的反应中,Cl元素被氧化,也被还原,故A错误;
B.稀硫酸中S为最高价,不具有强氧化性,一般来说,元素具有较高的价态,具有氧化性,故B错误;
C.HClO可分解生成HCl和氧气,Cl元素的化合价降低,O元素化合价升高,则HClO既有氧化性,又有还原性,故C正确;
D.氯气与水反应生成HCl、HClO,则该反应中1molCl2参加反应转移1mol电子,故D错误;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意结合实例分析,题目难度不大.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
13.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净化 | |
| B. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| C. | 金属的电化学腐蚀比化学腐蚀更普遍 | |
| D. | 电解MgCl2饱和溶液,可制得金属镁 |
12.下列溶液中能大量共存的离子组是( )
| A. | 加入铝粉能产生H2的溶液:Fe2+、NH4+、SO42-、NO3- | |
| B. | 室温下水电离出c(H+)=1×10-13 mol/L的溶液:HCO3-、K+、SO42-、Cl- | |
| C. | 使酚酞变红色的溶液:Na+、K+、AlO2-、CO32- | |
| D. | 含大量Fe3+的溶液:NH4+、Na+、SCN-、Cl- |
19.白磷分子如图所示:则31g白磷中存在的共价键数目为( )
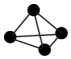

| A. | 4NA | B. | NA | C. | 1.5NA | D. | 0.25NA |
9.下列变化过程中原物质分子内的共价键被破坏,同时有离子键形成的是( )
| A. | 碘升华 | B. | 盐酸和氢氧化钠溶液混合 | ||
| C. | 氯化氢溶于水 | D. | 氯化氢与氨气反应生成氯化铵固体 |
13.要除去MnC12溶液中的Cu2十,Pb2+,Cd2+等金属离子,可通过添加过量难溶电解质MnS,使这些金属离子形成硫化物沉淀而除去.根据上述事实,可推知MnS具有的相关性质是( )
| A. | 具有吸附性 | B. | 溶解度与CuS、PbS、Cd相同 | ||
| C. | 溶解度小于CuS,PbS、Cd | D. | 溶解度大于CuS,PbS,CdS |
14.常温下,下列物质中能使铝发生钝化的是( )
| A. | 浓硫酸 | B. | 浓烧碱溶液 | C. | 浓盐酸 | D. | 浓氯化铁溶液 |