题目内容
200℃时,11.6gCO2和H2O(g)的混合气体与足量的Na2O2固体充分反应后,质量增加了3.6g,则原混合气体的平均相对分子质量为( )。A.5.8 B.21.6 C.23.2 D.46.4
C
【试题分析】
解析:设混合气体中CO2、H2O的物质的量分别为xmol、ymol,由题意得:28x+2y=3.6,44x+18y=11.6,解得:x=0.1,y=0.4,故n(CO2)∶n(H2O)=1∶4,所以Mr=
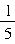 ×44+
×44+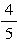 ×18=23.2。故选C。
×18=23.2。故选C。 
练习册系列答案
相关题目
 、
、 、
、 、
、 等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是
( )
等离子的水溶液中,若溶液体积保持不变,则下列说法中正确的是
( )