题目内容
6. 现有14.4g CO和CO2的混合气体,在标准状况下其体积为8.96L.回答下列问题:
现有14.4g CO和CO2的混合气体,在标准状况下其体积为8.96L.回答下列问题:(1)该混合气体的平均摩尔质量为36g/mol.
(2)混合气体中碳原子的个数为0.4NA(用NA表示阿伏伽德罗常数的值).
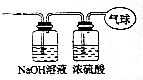
(3)将混合气体依次通过如图装置,最后收集在气球中(实验在标准状况下进行).
①气球中收集到的气体的摩尔质量为28g/mol.
②气球中收集到的气体中,电子总数为2.8NA(用NA表示阿伏伽德罗常数的值).
③气球中的体积为4.48L.
分析 (1)标况下混合气体的体积为8.96L,其物质的量为:n=$\frac{V}{Vm}$=$\frac{8.96L}{22.4L/mol}$=0.4mol,根据M=$\frac{m}{n}$计算出平均摩尔质量;
(2)设出一氧化碳、二氧化碳的物质的量,根据气体的总质量和总物质的量列方程式计算;
(3)将混合气体依次通过如图装置,则CO2会被NaOH溶液吸收,剩余CO,被浓硫酸干燥后,则在气球中收集到的是干燥纯净的CO气体.
①一种物质的摩尔质量在数值上等于该物质的相对分子质量;
②一个CO含有14个电子,由(2)求出的CO的物质的量计算电子的物质的量和数目;
③气球中的气体为CO,根据体积V=nVm来计算.
解答 解:(1)混合气体的体积为8.96L,则物质的量为其物质的量为:n=$\frac{V}{Vm}$=$\frac{8.96L}{22.4L/mol}$=0.4mol,
混合气体的平均摩尔质量为:$\frac{14.4g}{0.4mol}$=36g/mol,
故答案为:36g/mol;
(2)设混合气体中CO的物质的量为xmol,CO2的物质的量为ymol,则根据混合物的质量为14.4g可得:28x+44y=14.4 ①;
根据气体的物质的量为0.4mol可得:x+y=0.4 ②
解①②得:x=0.2mol、y=0.2mol.
由于CO和CO2中均含1个碳原子,故0.2molCO和0.2molCO2中共含0.4molC原子即0.4NA个,
故答案为:0.4NA;
(3)将混合气体依次通过如图装置,则CO2会被NaOH溶液吸收,剩余CO,被浓硫酸干燥后,则在气球中收集到的是干燥纯净的CO气体.
①气球中收集到的气体为CO,而一种物质的摩尔质量在数值上等于该物质的相对分子质量,故收集到气体的摩尔质量为28g/mol,
故答案为:28g/mol;
②一个CO含有14个电子,由(2)求出的CO的物质的量为0.2mol,则电子的物质的量为0.2mol×14=2.8mol,电子总数为2.8NA个;
故答案为:2.8NA;
③气球中的气体为CO,其体积V=nVm=0.2mol×22.4L/mol=4.48L,
故答案为:4.48.
点评 本题考查了有关混合物的计算、物质的量的有关计算,题目难度中等,为高频考点,试题侧重于学生的分析能力和计算能力的考查,注意质量守恒定律在化学计算中的应用方法.

 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案| A. | SO3溶于水能导电,故SO3属于电解质 | |
| B. | H2SO4是强电解质,H2SO4在水溶液里和熔融状态下,都能导电 | |
| C. | BaSO4难溶于水.故BaSO4属于弱电解质 | |
| D. | 氢离子浓度相同的盐酸和醋酸导电能力相同 |
| A. | 用溶解和过滤的方法提纯含有少量BaSO4的BaCO3 | |
| B. | 用分液的方法除去酒精中的少量水 | |
| C. | 用蒸馏的方法分离水和四氯化碳的混合物 | |
| D. | 用结晶的方法提纯含有少量KCl的KNO3晶体 |
| 离子种类 | Na+ | Cl- | NH4+ | SO42- |
| 离子浓度 | 2.3×10-5mol/L | 3.5×10-5mol/L | 7×10-6mol/L | 2.4×10-6mol/L |
(2)取1mL该酸雨,若完全反应消耗NaOH的物质的量为3.5×10-6mol.
(3)若只用一份该酸雨样品检验其中Cl-和SO42-应先加Ba(OH)2(填化学式)待沉淀完全后再加AgNO3(填化学式).
(4)在问题(3)中判断已沉淀完全可加第二份沉淀剂的具体操作方法为取加入氢氧化钡以后的溶液少量,向其中加入少量的盐酸,看是否产生无色气体,若没有气体产生,证明硫酸根离子沉淀完全.

| A. | 相对于途径①,途径②更好地体现了绿色化学思想 | |
| B. | Y可以是葡萄糖溶液 | |
| C. | 利用途径②制备16g硫酸铜,被还原的硫酸的物质的量为0.1mol | |
| D. | 途径①所用混酸中H2S04与HN03物质的量之比最好为3:2 |
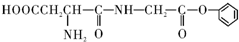 下列有关M的叙述中正确的是( )
下列有关M的叙述中正确的是( )| A. | M的分子式为:C12H15O5N2 | |
| B. | M可以发生水解反应、中和反应、加成反应、消去反应 | |
| C. | M的水解产物中一定含有醇类 | |
| D. | 1 molM最多可以与1L4mol/L的NaOH溶液完全反应 |