题目内容
下列不能用勒夏特列原理解释的是( )
| A、在配制FeCl2、FeCl3等溶液时,一般是将FeCl2、FeCl3等固体溶解在含少量HCl的溶液中,从而得到澄清的溶液 |
| B、除去CuCl2溶液中的Fe3+杂质时,通常是向其中加入CuO或Cu(OH)2等固体 |
| C、在一密闭容器中有一定量N2和H2,加入催化剂会使合成氨的速率加快 |
| D、常温下的醋酸溶液升温20℃,pH减小 |
考点:化学平衡移动原理
专题:化学平衡专题
分析:勒夏特利原理是如果改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动,勒夏特利原理适用的对象应存在可逆过程,如与可逆过程的平衡移动无关,则不能用勒夏特利原理解释.
解答:
解:A.存在水解平衡,盐酸溶液抑制铁离子和亚铁离子的水解,能用勒夏特列原理解释,故A不选;
B.Fe3+水解使溶液呈酸性,加入CuO或Cu(OH)2等固体可以与氢离子反应,使水解平衡正向移动,生成氢氧化铁沉淀,能用勒夏特列原理解释,故B不选;
C.催化剂只能加快反应速率,不能使平衡移动,不能用勒夏特列原理解释,故C选;
D.醋酸的电离过程是吸热过程,升高温度,电离平衡正向移动,氢离子浓度增大,pH减小,能用勒夏特列原理解释,故D不选;
故选C.
B.Fe3+水解使溶液呈酸性,加入CuO或Cu(OH)2等固体可以与氢离子反应,使水解平衡正向移动,生成氢氧化铁沉淀,能用勒夏特列原理解释,故B不选;
C.催化剂只能加快反应速率,不能使平衡移动,不能用勒夏特列原理解释,故C选;
D.醋酸的电离过程是吸热过程,升高温度,电离平衡正向移动,氢离子浓度增大,pH减小,能用勒夏特列原理解释,故D不选;
故选C.
点评:本题考查影响化学平衡移动的因素,难度不大.要熟练掌握勒夏特列原理.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
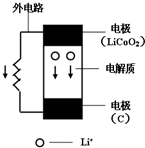 某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6
某新型二次锂离子电池结构如右图,电池内部是固体电解质,充电、放电时允许Li+在其间通过(图中电池内部“→”表示放电时Li+的迁移方向).充电、放电时总反应可表示为:Li1-xCoO2+LixC6| 充电 |
| 放电 |
| A、外电路上的“→”表示放电时的电流方向 |
| B、充电时阴极电极反应:LixC6-xe-═6C+xLi+ |
| C、放电时负极电极反应:LiCoO2-xe-═Li1-xCoO2+xLi+ |
| D、外电路有0.1mol e-通过,发生迁移的Li+的质量为0.7g |
下列关于乙醇的说法中,正确的是( )
| A、分子中含有C=O键 |
| B、官能团为羧基 |
| C、能使紫色石蕊试液变红 |
| D、可用碳酸钠溶液来鉴别乙醇和乙酸溶液 |
下列反应属于吸热反应的是( )
| A、C6H12O6(葡萄糖)+6O2═6CO2+6H2O |
| B、CH3COOH+KOH═CH3COOK+H2O |
| C、所有高温条件下发生的反应 |
| D、破坏生成物全部化学键所需能量小于破坏反应物全部化学键的能量 |
阿伏加德罗常数为NA,下列说法中正确的是( )
| A、1.0L 1.0 mol?L-1NaNO3溶液中含有的氧原子数为3NA |
| B、在标准状况下,22.4LCO2和O2混合气体中含有的氧原子数为NA |
C、 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA 31 g P4 (分子结构如图)中含有的P-P键个数为1.5NA |
| D、0.1mol Fe在0.1mol C12中充分燃烧,转移的电子数为0.3NA |
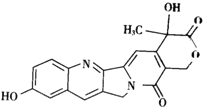 具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的就法错误的是( )
具有显著抗癌活性的10-羟基喜树碱的结构如图所示.下列关于10-羟基喜树碱的就法错误的是( )| A、该物质属于有机物 |
| B、该物质不属于烃 |
| C、该物质完全燃烧后的产物只有CO2和H2O |
| D、该物质中既含有极性键又含有非极性键 |
下列物质的分子中,只含有极性共价键的是( )
| A、氯化镁 | B、单质碘 | C、乙烷 | D、水 |
比较下列各组物质的沸点,正确的是( )
| A、乙醇>丙烷 |
| B、异戊烷>正戊烷 |
| C、1-丁烯>1-庚烯 |
| D、乙二醇>丙三醇 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、1L 0.1 mol?L-1的H2SO4溶液中粒子数为0.15NA |
| B、标准状况下,22.4L乙醇中含有的氧原子数为NA |
| C、1mol CO2分子中共用电子对数为2NA |
| D、23g Na与足量的O2完全反应,失去的电子数目为NA |