题目内容
从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物④将得到的产物熔融电解得到镁.下列说法不正确的是( )
| A、此法的优点之一是原料来源丰富 |
| B、①②③步骤的目的是从海水中提取MgCl2 |
| C、以上提取镁的过程中涉及化合、分解和复分解反应 |
| D、第④步电解时阴极产生氯气 |
考点:海水资源及其综合利用
专题:
分析:①把贝壳制成石灰乳,生成Ca(OH)2;
②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,生成Mg(OH)2;
③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物得到MgCl2;
④将得到的产物熔融电解得到镁,反应为:MgCl2
Mg+Cl2.
②在引入的海水中加入石灰乳,沉降、过滤、洗涤沉淀物,生成Mg(OH)2;
③将沉淀物与盐酸反应,结晶过滤、在HCl气体氛围中干燥产物得到MgCl2;
④将得到的产物熔融电解得到镁,反应为:MgCl2
| ||
解答:
解:A.海水资源丰富,海水中含有大量的镁元素,故A正确;
B.经过①②③步骤可得到MgCl2,故B正确;
C.贝壳的主要成分为CaCO3,加热分解生成CaO,CaO和水发生化合反应生成Ca(OH)2,与MgCl2发生复分解反应生成Mg(OH)2,故C正确;
D、第④步电解熔融氧化镁,产物为镁和氯气,MgCl2(熔融)
Mg+Cl2↑,但是氯气是失去电子,被氧化,应在阳极放电,故D错误;故选D.
B.经过①②③步骤可得到MgCl2,故B正确;
C.贝壳的主要成分为CaCO3,加热分解生成CaO,CaO和水发生化合反应生成Ca(OH)2,与MgCl2发生复分解反应生成Mg(OH)2,故C正确;
D、第④步电解熔融氧化镁,产物为镁和氯气,MgCl2(熔融)
| ||
点评:本题主要考查了从海水中提取镁,掌握相关的化学反应原理是解答的关键,题目较简单.

练习册系列答案
相关题目
某有机物 的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )
的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )
 的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )
的同分异构体X,X分子中含有苯环,且苯环上一氯代物只有两种,则X的可能结构有( )| A、3种 | B、4 种 |
| C、5种 | D、6种 |
下列实验过程中,始终无明显现象的是( )
| A、SO2通入BaCl2溶液中 |
| B、CO2通入饱和Na2CO3溶液中 |
| C、NH3通入FeCl3溶液中 |
| D、Cl2通入KI溶液中 |
甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲
乙
丙.下列有关物质的推断不正确的是( )
| 丁 |
| 丁 |
| A、若甲为焦炭,则丁可能是O2 |
| B、若甲为SO2,则丁可能是氢氧化钠溶液 |
| C、若甲为Fe,则丁可能是浓盐酸 |
| D、若甲为AgNO3溶液,则丁可能是氨水 |
常温下的定容容器中,建立如下平衡:3NO2+H2O?NO+2HNO3,在其他条件不变时,若往容器中通入少量的O2后、原体系将会发生的变化是( )
| A、平衡向逆反应方向移动 |
| B、NO的物质的量可能不变 |
| C、NO的物质的量一定会减少 |
| D、NO2增加的物质的量是通入的物质的量的2倍 |
分类是化学学习和研究中的常用手段,下列分类依据和结论都正确的是( )
| A、浓盐酸、浓硫酸、浓硝酸均具有氧化性,都属氧化性酸 |
| B、Na2O、SO2、BaSO4在熔融状态或溶于水时均能导电,都属电解质 |
| C、NaOH、HNO3、NaNO3在水溶液中均能电离出离子,都属离子化合物 |
| D、NaOH、Na2CO3、NaCl、Na2SO4可按某种标准划为一类物质,分类标准是可溶于水 |
下列叙述正确的是( )
| A、元素周期表中位于金属与非金属分界线附近的元素属于过渡元素 |
| B、短周期第IVA族与VIIA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
| C、C、N、O、H四种元素形成的化合物一定既有离子键又有共价键 |
| D、第三周期非金属元素含氧酸的酸性从左到右依次增强 |
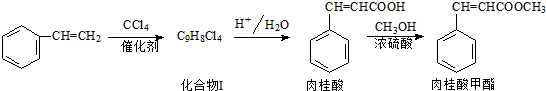
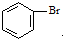 和CH=CHCOOH反应制得,该反应的反应类型是
和CH=CHCOOH反应制得,该反应的反应类型是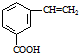 )是肉桂酸的同分异构体,下列有关化合物II和肉桂酸的说法正确的是
)是肉桂酸的同分异构体,下列有关化合物II和肉桂酸的说法正确的是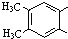 ,它在稀硫酸中能水解,且水解产物经聚合反应后得到高聚物.化合物Ⅲ有多种结构,写出其中一种的结构简式
,它在稀硫酸中能水解,且水解产物经聚合反应后得到高聚物.化合物Ⅲ有多种结构,写出其中一种的结构简式