题目内容
【题目】氯碱工业是以电解饱和食盐水为基础的化学工业。
I.电解所用的氯化钠溶液需精制,除去有影响的Ca2+、Mg2+、NH4+、SO42-及泥沙,其精制流程如下:
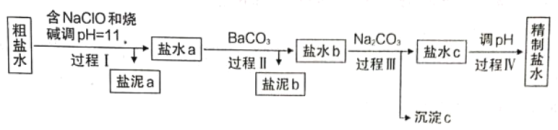
已知:①Ca2+、Mg2+开始形成相应氢氧化物沉淀的pH如下表。
Ca(OH)2 | Mg(OH)2 | |
pH | ≥11.5 | ≥9.2 |
②Ksp(BaSO4)= 1.1×10-10,Ksp(BaCO3)=2.6×10-9,Ksp(CaCO3)=5.0×10-9。
(1)盐泥a除泥沙外,还含有____________________________________。
(2)过程I中,NaClO的作用是将NH4+转化为N2,反应的离子方程式为________________________。
(3)过程III中,沉淀c主要成分的化学式为________________________。
(4)过程IV调pH目的是____________。
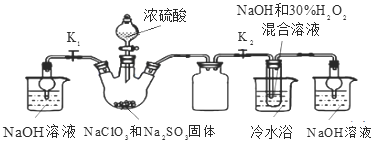
II.如图是将电解池与燃料电池相组合电解精制饱和食盐水的新工艺,可以节(电)能30%以上。相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
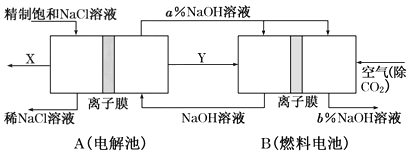
(1)图中X是____________(填化学式)。
(2)Y在装置B中发生的电极反应式为____________。
(3)写出A装罝中发生的总反应离子方程式____________,比较图示中氧氧化钠溶液质量分数a%与b%的大小:________________________。
(4)若用装置B作为装置A的辅助电源,每当消耗标准状况下氧气的体积为11.2L时,则装置B可向装置A提供的电量约为____________(一个e-的电量为1.60×10-19C;计算结果精确到0.01)。
【答案】含有Mg(OH)2 3C1O-+2 NH4++2OH-=3Cl-+ N2↑+5H2O CaCO3 除去多余的CO32-和OH- Cl2 H2-2e-+2OH-=2H2O 2Cl-+2H2O![]() Cl2↑+H2↑+2OH- b%>a% 1.93×105C
Cl2↑+H2↑+2OH- b%>a% 1.93×105C
【解析】
Ⅰ除去有影响的Ca2+、Mg2+、NH4+、SO42-及泥沙,过程Ⅰ加入NaClO和烧碱后调pH=11,可以除去泥沙和Mg2+,NaClO的作用是将NH4+转化为N2,可以除去NH4+,盐水a中含有Ca2+、SO42-。根据已知②可知,加入BaCO3后,由于BaSO3的Ksp小于BaSO4的Ksp,所以BaCO3会转化为BaSO4,从而除去SO42-,但Ca2+没有除去。盐泥b中有BaSO4,盐水b中有Ca2+和少量的CO32-。过程Ⅲ可以除去Ca2+,沉淀c是CaCO3,过程Ⅳ可以通过调pH(即加入盐酸)除去CO32-和OH-,得到精制盐水。
ⅡA装置是电解池,B装置是原电池。电解氯化钠溶液的生成物是氯气、氢气和氢氧化钠,所以X是氯气,Y是氢气,在装置B中做负极,失电子;氧气在正极通入得电子。
Ⅰ(1)根据表格可知,pH=11时,Mg(OH)2开始沉淀,Ca(OH)2没有沉淀,所以盐泥中还有Mg(OH)2。
(2)NaClO与NH4+反应生成N2,氮元素的化合价升高,次氯酸根中氯的化合价降低到-1,配平得到离子方程式为3C1O-+2 NH4++2OH-=3Cl-+ N2↑+5H2O。
(3)根据分析可知,沉淀c是CaCO3。
(4)根据分析可知,过程Ⅳ的作用是除去多余的CO32-和OH-。
Ⅱ(1)根据分析可知, X是Cl2。
(2)氢气在负极发生的电极反应式为H2-2e-+2OH-=2H2O。
(3)A装罝中阳极是Cl-失去电子生成Cl2,阴极是水电离的H+得到电子生成H2,发生的总反应离子方程式是2Cl-+2H2O![]() Cl2↑+H2↑+2OH-。从电解池产生的a%的NaOH进入原电池中,在原电池的正极上氧气得到电子:O2+4e-+2H2O=4OH-, OH-浓度增大,Na+又通过离子膜移动到正极室,所以正极室中NaOH溶液的浓度增大,因此b%>a%。故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-。从电解池产生的a%的NaOH进入原电池中,在原电池的正极上氧气得到电子:O2+4e-+2H2O=4OH-, OH-浓度增大,Na+又通过离子膜移动到正极室,所以正极室中NaOH溶液的浓度增大,因此b%>a%。故答案为:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-,b%>a%。
Cl2↑+H2↑+2OH-,b%>a%。
(4)消耗标准状况下氧气的体积为11.2L(即0.5mol)时,转移电子2mol,则装置B可向装置A提供的电量约为2mol×6.02×![]() ×1.60×10-19C= 1.93×105C。
×1.60×10-19C= 1.93×105C。

 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案