题目内容
15.下列反应体现了CO2的氧化性是( )| A. | O2+C$\frac{\underline{\;高温\;}}{\;}$CO2 | B. | 2NaOH+CO2═Na2CO3+H2O | ||
| C. | 2Na2O2+CO2═2Na2CO3+O2 | D. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C |
分析 反应中存在元素化合价的变化的反应属于氧化还原反应,氧化还原反应中CO2的C元素的化合价降低,作氧化剂,体现氧化性,据此分析.
解答 解:A.O2+C$\frac{\underline{\;高温\;}}{\;}$CO2反应中C元素的化合价升高,体现了C的还原性,故A错误;
B.2NaOH+CO2═Na2CO3+H2O反应中没有元素化合价的变化,不是氧化还原反应,故B错误;
C.2Na2O2+CO2═2Na2CO3+O2反应中C元素的化合价没有变化,不体现CO2的氧化性,故C错误;
D.2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C反应中CO2的C元素的化合价降低,作氧化剂,体现氧化性,故D正确.
故选D.
点评 本题考查了氧化还原反应,侧重于基础知识的考查,题目难度不大,注意从化合价变化的角度分析.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
5. 早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )
早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )
 早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )
早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )| A. | [18]-轮烯分子中所有原子不可能处于同一平面 | |
| B. | 1mol-[18]轮烯最多可与9mol氢气发生加成反应生成环烷烃 | |
| C. | [18]-轮烯的分子式为:C18H12 | |
| D. | [18]-轮烯与乙烯互为同系物 |
6.下列可证明甲烷分子是正四面体结构的是( )
| A. | 一氯甲烷没有同分异构体 | B. | 甲烷分子的四个键完全不相同 | ||
| C. | 甲烷分子的四个键完全相同 | D. | 二氯甲烷没有同分异构体 |
3.经测定,由C3H7OH和C6H12组成的混合物中氢的质量分数为14%,则此混合物中碳的质量分数为( )
| A. | 78% | B. | 22% | C. | 14% | D. | 13% |
10.下列关于镁的叙述正确的是( )
| A. | 镁条失火可以用CO2进行扑灭 | B. | 镁不能与稀硫酸反应放出H2 | ||
| C. | 镁制容器可以盛放浓硝酸 | D. | 镁在空气中燃烧产物并不全是MgO |
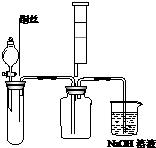 (1)某同学为了证明并观察到铜与稀硝酸反应的产物NO,实验时首先向下图试管中加入一定量的块状固体,再滴加过量的稀硝酸,待反应产生的气体充满试管后,再将铜丝插入稀硝酸溶液中.你认为试管中的块状固体是碳酸钙,其作用是赶走试管中的空气,实验结束时,用注射器向试管内推入氧气(或空气)的目的是检验NO,观察到红棕色气体.
(1)某同学为了证明并观察到铜与稀硝酸反应的产物NO,实验时首先向下图试管中加入一定量的块状固体,再滴加过量的稀硝酸,待反应产生的气体充满试管后,再将铜丝插入稀硝酸溶液中.你认为试管中的块状固体是碳酸钙,其作用是赶走试管中的空气,实验结束时,用注射器向试管内推入氧气(或空气)的目的是检验NO,观察到红棕色气体.