题目内容
【题目】在恒容密闭容器中存在如下反应。2A(g)+B(g)![]() 3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是( )
3C(g)+D(s) H<0,在其他条件不变时,改变某一条件对上述平衡的影响,下列分析正确的是( )
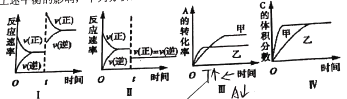
A.图Ⅰ表示增加生成物浓度对该平衡的影响
B.图Ⅱ表示增大压强对该平衡的影响
C.图Ⅲ表示温度对该平衡的影响,温度:乙>甲
D.图Ⅳ表示催化剂对该平衡的影响,催化效率:乙>甲
【答案】C
【解析】
A. 图Ⅰ中正逆反应速率都增大,不能表示增加生成物浓度对该平衡的影响,故错误;
B. 图Ⅱ表示改变条件后正逆速率都降低,但平衡不移动,说明表示减小压强对该平衡无影响,故错误;
C. 图Ⅲ表示温度对该平衡的影响,升温,平衡逆向移动,A的转化率降低,故温度:乙>甲,故正确;
D. 图Ⅳ表示改变条件改变速率,但平衡不移动,所以可以表示催化剂对该平衡的影响,且催化效率:甲>乙 ,故错误;
故选C。

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) ![]() 2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。平衡时G的体积分数(%)随温度和压强的变化如下表所示:
温度/体积分数/压强 | 1.0 | 2.0 | 3.0 |
810 | 54.0 | a | B |
915 | c | 75.0 | D |
1000 | E | f | 83.0 |
①b<f ②915 ℃、2.0 MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1 000 ℃)>K(810 ℃) 上述①~④中正确的 ( )
A.①②B.②③C.②③④D.①②③④
【题目】800°C时,在2L密闭容器中发生反应2NO(g)+O2(g)![]() 2NO2(g) H<0,测得n(NO)随时间的变化如下表:
2NO2(g) H<0,测得n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.20 | 0.10 | 0.08 | 0.07 | 0.07 | 0.07 |
(1)NO的平衡浓度c(NO)=____________________。
(2)下图中表示NO2的变化的曲线______________。(填字母)
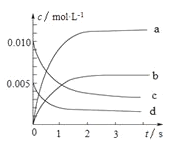
(3)能说明该反应已经达到化学平衡状态的是______________。
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.v逆(NO)=v正(O2) D.容器内NO、O2、NO2同时存在
(4)下列操作中,能使该反应的反应速率增大,且平衡向正反应方向移动的是________。
A.及时分离出NO2气体B.适当升高温度
C.增大O2的浓度D.选择高效的催化剂
(5)下图中的曲线表示的是其它条件一定时,体系中NO的平衡转化率与温度的关系。图中标有a、b、c、d四点,其中表示v(正)<v(逆)的点是____________。(填选项)
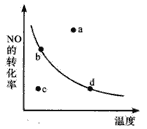
A.a B.b C.c D.d
【题目】下列表格中的各种情况,可以用对应选项中的图像表示的是
选项 | 反应 | 甲 | 乙 |
A | 外形、大小相近的金属和水反应 | Na | K |
B | 4mL0.01mol·L-1 KMnO4溶液分别和不同浓度的2mLH2C2O4(草酸)溶液反应 | 0.1mol·L-1的H2C2O4溶液 | 0.2mol·L-1的H2C2O4溶液 |
C | 5mL0.1mol·L-1Na2S2O3溶液和5mL0.1mol·L-1H2SO4溶液反应 | 热水 | 冷水 |
D | 5mL4%的过氧化氢溶液分解放出O2 | 无MnO2粉末 | 加MnO2粉末 |
A.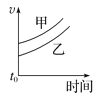 B.
B.
C. D.
D.