题目内容
【题目】在周期表中找到第3横行17纵行的元素,回答下列问题:
(1)该元素的符号是________,其原子结构示意图为________
(2)该元素位于第________周期,第________族。
(3)写出下列反应的化学方程式:
①该元素的单质+水:_______________________________________;
②该元素的单质+氢氧化钠:_________________________________。
【答案】 Cl 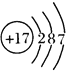 三 ⅦA Cl2+H2O====HCl+HClO Cl2+2NaOH===NaCl+NaClO+H2O
三 ⅦA Cl2+H2O====HCl+HClO Cl2+2NaOH===NaCl+NaClO+H2O
【解析】(1)元素周期表中第3横行17纵行的元素是第三周期第ⅤⅡA族的Cl元素,属于非金属元素,原子结构示意图为: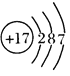 ;(2)元素周期表中行数等于周期数,纵行数等于族序数,第3横行17纵行即为第三周期,第VIIA族;(3)①氯气能和水反应,即Cl2+H2O=HCl+HClO;②能和烧碱反应,可以用来进行尾气处理,即Cl2+NaOH=NaCl+NaClO+H2O。
;(2)元素周期表中行数等于周期数,纵行数等于族序数,第3横行17纵行即为第三周期,第VIIA族;(3)①氯气能和水反应,即Cl2+H2O=HCl+HClO;②能和烧碱反应,可以用来进行尾气处理,即Cl2+NaOH=NaCl+NaClO+H2O。

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案【题目】下表是元素周期表的一部分, 针对表中的①~⑧种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)在这些元素中,化学性质最不活泼的是:______(填具体元素符号,下同)。原子结构示意图为________________ 。元素⑦名称为_______在周期表中的位置________________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的化学式是:_____________。
(3)最高价氧化物是两性氧化物的元素是__________;写出它的氧化物与氢氧化钠反应的离子方程式__________________________________________________。
(4)③、⑥、⑦三种元素形成的离子,离子半径由大到小的顺序是(写元素符号)______________。
(5)元素③的氢化物的化学式为________;该氢化物常温下和元素⑦的单质反应的化学方程式为______________________。
(6)写出⑥的最高价氧化物的水化物和①反应的化学方程式:_______________。