题目内容
A、B、C 3种元素的核外电子数都比氩原子少,若A和C处于同一主族,A和B的核电荷数之差为5,B原子的M电子层比L电子层少2个电子,则A、B、C 3种元素可能分别为( )
| A、Li、Na、S |
| B、Na、S、Li |
| C、Na、K、Br |
| D、K、Br、Na |
考点:原子结构与元素的性质
专题:元素周期律与元素周期表专题
分析:A、B、C 3种元素的核外电子数都比氩原子少,B原子的M电子层比L电子层少2个电子,原子M层电子数=8-2=6,则B为S,A和B的核电荷数之差为5,则A核电荷数=16-5=11,故A为Na,若A和C处于同一主族,则A为H或Li,据此解答.
解答:
解:A、B、C 3种元素的核外电子数都比氩原子少,B原子的M电子层比L电子层少2个电子,原子M层电子数=8-2=6,则B为S,A和B的核电荷数之差为5,则A核电荷数=16-5=11,故A为Na,若A和C处于同一主族,则A为H或Li,选项中只有B符合,
故选B.
故选B.
点评:本题考查原子结构与位置关系,比较基础,根据核外电子排布推断B元素是关键.

练习册系列答案
相关题目
金属汞在加热条件下可以与氧气化合生成氧化汞,反应如下:2Hg+O2=2HgO,下列哪个选项可以说明0.3mol Hg 与0.1mol O2 充分反应后物质的种类及其量的情况?( )
| A、0.2molHgO+0.1molHg |
| B、0.2molHgO |
| C、0.2molHgO+0.1molO2 |
| D、0.1molHgO+0.1molHg |
下列物质的水溶液能导电,但其本身属于非电解质的是( )
| A、C2H5OH |
| B、CO2 |
| C、Cl2 |
| D、BaSO4 |
环境污染已成为人类社会面临的重大威胁.下列物质与环境问题对应关系不正确的是( )
| A、酸雨,二氧化硫 |
| B、温室效应,二氧化碳 |
| C、白色污染,二氧化硅 |
| D、臭氧层空洞,氟氯代烷 |
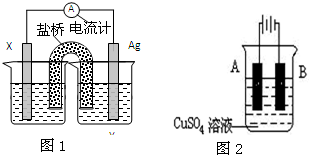 (Ⅰ)依据氧化还原反应:2Ag+(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计的原电池如图1所示.
(Ⅰ)依据氧化还原反应:2Ag+(aq)+Fe(s)=Fe2+(aq)+2Ag(s)设计的原电池如图1所示.