题目内容
12.已知2NaHCO3$\frac{\underline{\;△\;}}{\;}$Na2CO3+CO2↑+H2O,现将1mol过氧化钠与2mol碳酸氢钠固体混合后,在密闭的容器中加热,充分反应,排出气体物质后冷却,残留的固体物质是( )| A. | Na2CO3 | B. | Na2O2、Na2CO3 | ||
| C. | NaOH、Na2CO3 | D. | Na2O2、NaOH、Na2CO3 |
分析 碳酸氢钠不稳定,加热易分解,发生反应:2NaHCO3$\frac{\underline{\;△\;}}{\;}$Na2CO3+CO2↑+H2O,2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2,由于二氧化碳与氢氧化钠反应生成碳酸钠,可以认为过氧化钠先与二氧化碳反应,再与水反应,结合物质的物质的量解答
解答 解:由方程式:2NaHCO3$\frac{\underline{\;△\;}}{\;}$Na2CO3+CO2↑+H2O,可知2mol NaHCO3分解得到Na2CO3、CO2和H2O各1mol,
还会发生反应:2Na2O2+2CO2=2Na2CO3+O2,2Na2O2+2H2O=4NaOH+O2,由于二氧化碳与氢氧化钠反应生成碳酸钠,可以认为过氧化钠先与二氧化碳反应,再与水反应,Na2O2只有1mol,恰好和CO2反应生成1molNa2CO3和O2,气体排出后,只剩余Na2CO3,
故选A.
点评 本题考查混合物反应的计算,题目难度中等,明确发生的反应为解答关键,注意理解“过氧化钠先与二氧化碳反应,再与水反应”,试题培养了学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
8.下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl2溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入过量CO2.
①金属钠投入到FeCl2溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中通入过量CO2
⑤向饱和Na2CO3溶液中通入过量CO2.
| A. | ①②③④⑤ | B. | 只有①④ | C. | 只有②③ | D. | 只有③④⑤ |
3.在一个2L的密闭容器中,某一反应物的物质的量为1.0mol,经过20s后,它的物质的量变成了0.6mol,在这20s内它的反应速率为( )
| A. | 0.4mol/L | B. | 0.02mol/(L•s) | C. | 0.01mol/L | D. | 0.01mol/(L•s) |
7.关于化学键的下列叙述正确的是( )
| A. | 化学键既存在于相邻原子间又存在于相邻分子间 | |
| B. | 两个原子间的相互作用叫化学键 | |
| C. | 化学键通常指的是相邻的两个或多个原子之间的强烈的相互作用 | |
| D. | 化学键的实质是静电吸引 |
17.把VL含有MgSO4和K2SO4的混合溶液分成两份,一份加入a mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡;另一份加入含b mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁.则原混合溶液中钾离子的浓度为( )mol/L.
| A. | 2b-$\frac{a}{v}$ | B. | 2a-$\frac{b}{v}$ | C. | $\frac{2(2b-a)}{v}$ | D. | $\frac{2(2a-b)}{v}$ |
4.将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)?2G(g).忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示.
①b<f②915℃,2.0MPa时E的转化率为60%③该反应的△S<0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
| 压强/MPa G体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
上述①~④中正确的有( )
| A. | 4个 | B. | 3个 | C. | 2个 | D. | 1个 |
1.下列四种X溶液,分别放入盛有10mL 2mol•L -1HCl的烧杯中,加水稀释至50mL,X和HCl进行反应,其中反应速率最大的是( )
| A. | 20mL3mol•L -1X的溶液 | B. | 20mL2mol•L -1X的溶液 | ||
| C. | 10mL4mol•L -1X的溶液 | D. | 10mL2mol•L -1X的溶液 |
2.某电化学装置工作原理如图,下列有关说法正确的是( )
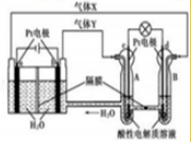

| A. | 气体X为O2 | |
| B. | c电极为负极,发生的电极反应式为H2-2e-=2H+ | |
| C. | 一段时间后A处PH降低 | |
| D. | 当有0.4mol电子转移时,在B极上生成标准状况下气体2.24L |