题目内容
4.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.现有一种无色的鲜花营养液,可能由硝酸钙、碳酸钾、硝酸钾、氯化钾中的一种或几种物质组成,为探究其成分,某同学设计并完成了如图所示的实验.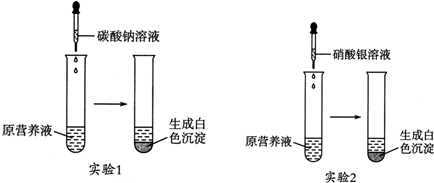
根据以上实验,请你填空.
①由实验1可确定原营养液中一定没有的物质是K2CO3(填化学式),写出生成白色沉淀的化学方程式是Ca(NO3)2+Na2CO3↓=CaCO3↓+2NaNO3.
②若测得原营养液中K+、Cl-的数目之比为2:1,则原营养液是由3种溶质配制成的.
③某同学用氯化钙、硝酸钾、氯化钾配成的营养液中K+、Cl-、NO3的数目之比为2:5:1,则所用硝酸钾和氯化钙的物质的量之比是1:2.
分析 ①根据硝酸钙、碳酸钾、硝酸钾、氯化钾几种物质中,硝酸钙可与碳酸钠生成白色碳酸钙沉淀进行解答;
②根据硝酸钙、硝酸钾、氯化钾几种物质中,氯化钾可与硝酸银生成白色氯化银沉淀,根据氯化钾溶液中钾离子与氯离子的个数比为1:1以及原营养液中K+、Cl-的数目之比为2:1进行解答;
③根据氯化钙、硝酸钾、氯化钾中含有的离子数目来回答.
解答 解:①根据如图所示的实验1,向营养液中滴加碳酸钠溶液出现白色沉淀,可判断原营养液中一定含有硝酸钙;而硝酸钙与碳酸钾不能在同一溶液中共存,因此可判断原营养液中一定不含碳酸钾;硝酸钙可与碳酸钠生成白色碳酸钙沉淀,化学方程式是Ca(NO3)2+Na2CO3↓=CaCO3↓+2NaNO3;
故答案为:K2CO3;Ca(NO3)2+Na2CO3↓=CaCO3↓+2NaNO3;
②根据如图所示的实验2,向营养液中滴加硝酸银溶液出现白色沉淀,可判断营养液中一定含有氯化钾,氯化钾可与硝酸银生成白色氯化银沉淀,离子方程式是Ag++Cl-=AgCl↓;如果原营养液是硝酸钙与氯化钾的混合溶液,溶液中的钾离子与氯离子个数比只能为1:1,而测定结果营养液中钾离子与氯离子个数比为2:1,因此,原营养液中还应含有硝酸钾;综上所述,原营养液应是硝酸钙、氯化钾、硝酸钾三种物质的混合溶液;
故答案为:3;
③设氯化钙、硝酸钾、氯化钾的物质的量分别是x、y、z,K+、Cl-、NO3-的数目之比等于物质的量之比,即为2:5:1,则钾离子的物质的量为y+z,氯离子的物质的量为:2x+z,硝酸根离子的物质的量为y,则 $\frac{y+z}{y}$=$\frac{2}{1}$,即y=z,则$\frac{2x+z}{y}$=$\frac{2x+z}{z}$=$\frac{5}{1}$,即x=2z,所以y:x=1:2,
故答案为:1:2.
点评 本题考查了物质的推断,题目难度中等,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用、以及物质的溶解性如常见的钾盐、钠盐、铵盐、硝酸盐都是可溶性盐,而氯化银、大多数的碳酸盐都不溶.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. | 胶头滴管伸入量筒内滴加液体 | |
| B. | 用酒精灯的外焰给盛有液体(液体体积约占试管体积的$\frac{1}{4}$)的试管加热 | |
| C. | 称量完药品后,将药匙内剩余的药品放回试剂瓶 | |
| D. | 过滤时漏斗的末端在烧杯的中央 |
| A. | 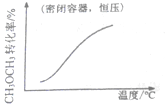 CH3OCH3(g)+3H2O(g)?6H2(g)+2CO2(g):△H>0 | B. | 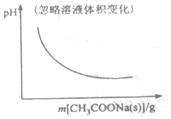 CH3COOH?H++CH3COO- | ||
| C. | 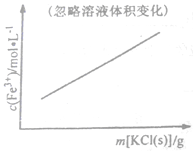 FeCl3+3KSCN?Fe(SCN)3+3KCl | D. |  N2(g)+3H2(g)?2NH3(g) |
| A. | 1:1 | B. | 3:2 | C. | 2:3 | D. | 3:4 |
| A. | 1 mol OH-中含有9NA个电子 | |
| B. | 常温下,23 g NO2和N2O4的混合气体中含有NA个氧原子 | |
| C. | 1 L 1 mol/L AlCl3溶液中含有NA个Al3+ | |
| D. | 常温常压下,11.2 L甲烷气体中含有的分子数为0.5NA |
| A. | NaOH、KOH | B. | NaOH、Cu(OH)2 | C. | Fe(OH)2、Cu(OH)2 | D. | Fe(OH)2、Fe(OH)3 |
 科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇(CH3OH),并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1
科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇(CH3OH),并开发出直接以甲醇为燃料的燃料电池.已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1和-726.5kJ•mol-1