题目内容
14.两种碱的混合物共8g与100mL2mol/L的盐酸恰好完全反应,则混合物组成可能是( )| A. | NaOH、KOH | B. | NaOH、Cu(OH)2 | C. | Fe(OH)2、Cu(OH)2 | D. | Fe(OH)2、Fe(OH)3 |
分析 100mL2mol/L的盐酸溶液中氯离子物质的量n=0.1L×2mol/L=0.2mol,结合氯元素守恒计算分析判断,
解答 解:A.NaOH、KOH物质的量分别为x、y,x+y=0.2mol,40x+56y=8,y=0,故A错误;
B.NaOH、Cu(OH)2 物质的量分别为x、y,x+2y=0.2mol,40x+98y=8,y=0,故B错误;
C.Fe(OH)2、Cu(OH)2物质的量分别为x、y,2x+2y=0.2mol,90x+98y=8,y<0,故C错误;
D.Fe(OH)2、Fe(OH)3物质的量分别为x、y,2x+3y=0.2mol,90x+107y=8,x=0.05,y=$\frac{1}{28}$,混合物组成可能是Fe(OH)2、Fe(OH)3,故D正确;
故选D.
点评 本题考查了混合物组成的分析计算,注意元素守恒的应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
5.现有下列短周期元素性质的数据:
(1)上述元素中处于同一主族的有③和⑥、④和⑦;处于第3周期的有②④⑤⑥⑧;(以上均用编号表示).
(2)已知A元素原子的M层上的电子数是K层电子数的3倍,则A在周期表中位置为第3周期ⅥA族;
B元素原子的次外层电子数是最外层电子数的$\frac{1}{4}$,则B原子的结构示意图为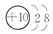 .
.
(3)三氧化铀是一种两性氧化物,它在溶液中可以以UO22+和U2O72-形式存在,按要求写出UO3与强酸、强碱反应的离子方程式:
①UO3与强碱反应2UO3+2OH-=U2O72-+H2O;
②UO3与强酸反应UO3+2H+=UO22++H2O.
 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10 m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 1.43 |
| 最高正化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负化合价 | -2 | -3 | -1 | -3 |
(2)已知A元素原子的M层上的电子数是K层电子数的3倍,则A在周期表中位置为第3周期ⅥA族;
B元素原子的次外层电子数是最外层电子数的$\frac{1}{4}$,则B原子的结构示意图为
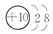 .
.(3)三氧化铀是一种两性氧化物,它在溶液中可以以UO22+和U2O72-形式存在,按要求写出UO3与强酸、强碱反应的离子方程式:
①UO3与强碱反应2UO3+2OH-=U2O72-+H2O;
②UO3与强酸反应UO3+2H+=UO22++H2O.
19.在aXm+和bYn-两种简单离子(X、Y都是短周期元素)中,已知Yn-比Xm+多两个电子层,下列关系或说法正确的是( )
| A. | X只能是第二周期的元素 | B. | a一定比b小 | ||
| C. | b-a+m+n一定等于16 | D. | Y只能是第三周期的元素 |
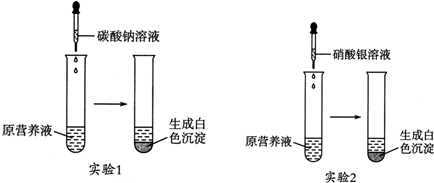
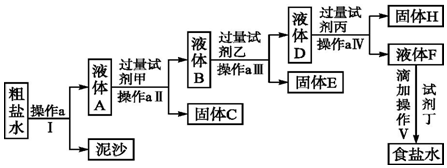

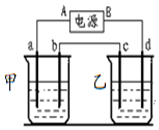 按如图的实验装置进行实验,其中a、b、c、d均为惰性电极.电解质溶液分别为硫酸铜和饱和氯化钠溶液,通电一段时间后,根据下列现象作出判断:【假设电解质均足量】
按如图的实验装置进行实验,其中a、b、c、d均为惰性电极.电解质溶液分别为硫酸铜和饱和氯化钠溶液,通电一段时间后,根据下列现象作出判断:【假设电解质均足量】