题目内容
将等物质的量的乙酸、乙二酸、某种饱和一元醛的混合物41.6g跟足量的金属钠反应,生成6.72L氢气(标准状况).则该醛分子中的碳原子数为( )
| A、5 | B、4 | C、3 | D、2 |
考点:化学方程式的有关计算
专题:计算题
分析:乙酸、乙二酸可与钠反应生成氢气,饱和一元醛与Na不反应,生成氢气为
=0.3mol,结合发生的反应2CH3COOH+2Na→2CH3COONa+H2↑、HOOC-COOH+2Na→NaOOC-COONa+H2↑及质量关系计算.
| 6.72L |
| 22.4L/mol |
解答:
解:生成氢气为
=0.3mol,设有机物的物质的量均为x,
2CH3COOH+2Na→2CH3COONa+H2↑
x 0.5x
HOOC-COOH+2Na→NaOOC-COONa+H2↑
x x
则0.5x+x=0.3,解得x=0.2mol,
乙酸、乙二酸的质量和为0.2mol×60g/mol+0.2mol×90g/mol=30g,
所以饱和一元醛的质量为41.6g-30g=11.6g
饱和一元醛的摩尔质量为
=58g/mol,
饱和一元醛的通式:CnH2nO,所以12n+2n+16=58,解得n=3,
则该醛分子中的碳原子数为3,
故选C.
| 6.72L |
| 22.4L/mol |
2CH3COOH+2Na→2CH3COONa+H2↑
x 0.5x
HOOC-COOH+2Na→NaOOC-COONa+H2↑
x x
则0.5x+x=0.3,解得x=0.2mol,
乙酸、乙二酸的质量和为0.2mol×60g/mol+0.2mol×90g/mol=30g,
所以饱和一元醛的质量为41.6g-30g=11.6g
饱和一元醛的摩尔质量为
| 11.6g |
| 0.2mol |
饱和一元醛的通式:CnH2nO,所以12n+2n+16=58,解得n=3,
则该醛分子中的碳原子数为3,
故选C.
点评:本题考查化学方程式的计算,侧重于学生的分析能力和计算能力的考查,为高频考点,把握有机物的性质及发生的反应结合质量守恒为解答的关键题,注意相关计算公式的运用,题目难度不大.

练习册系列答案
相关题目
下列各项表达式正确的是( )
A、N2的电子式: |
B、H2O2的电子式: |
C、NaCl的电子式: |
D、F-的结构示意图: |
X+的核外各层电子数分别为2、8,则X元素在周期表中的位置是( )
| A、第2周期第0族 |
| B、第3周期第ⅠA族 |
| C、第2周期第ⅠA族 |
| D、第2周期第ⅦA族 |
下列制取硝酸铜的方法中符合绿色化学理念的是( )
| A、氧化铜和稀硝酸反应 |
| B、铜和稀硝酸反应 |
| C、铜和硝酸铁溶液反应 |
| D、铜和浓硝酸反应 |
按要求填空
(1)最简单烯烃的结构简式: ;
(2)相对分子质量最小的有机物的结构式: ;
(3)乙烯与溴化氢反应方程式: ,反应类型 ;
(4)在浓硫酸作用下,苯与浓硝酸在60℃反应方程式: ,反应类型 .
(1)最简单烯烃的结构简式:
(2)相对分子质量最小的有机物的结构式:
(3)乙烯与溴化氢反应方程式:
(4)在浓硫酸作用下,苯与浓硝酸在60℃反应方程式:
如图为香芹酮分子的结构,下列有关叙述正确的是( )


| A、香芹酮化学式为C9H12O |
| B、香芹酮可以发生加成反应、消去反应和氧化反应 |
| C、香芹酮能使酸性KMnO4溶液退色 |
| D、香芹酮分子中有3种官能团 |

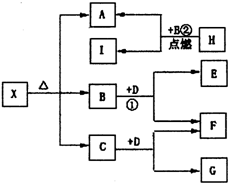 已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.
已知X是一种盐,H是常见金属单质,F、I是常见非金属单质,E、G都是工业上重要的碱性物质,它们有如图所示的关系.