题目内容
X+的核外各层电子数分别为2、8,则X元素在周期表中的位置是( )
| A、第2周期第0族 |
| B、第3周期第ⅠA族 |
| C、第2周期第ⅠA族 |
| D、第2周期第ⅦA族 |
考点:元素周期表的结构及其应用
专题:
分析:X+的核外各层电子数分别为2、8,则质子数为2+8+1=11,为钠元素,以此来解答.
解答:
解:X+的核外各层电子数分别为2、8,则质子数为2+8+1=11,为钠元素,原子结构为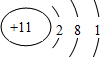 ,由3个电子层可知,位于第三周期,由最外层电子数可知,位于第IA族,
,由3个电子层可知,位于第三周期,由最外层电子数可知,位于第IA族,
故选B.
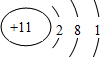 ,由3个电子层可知,位于第三周期,由最外层电子数可知,位于第IA族,
,由3个电子层可知,位于第三周期,由最外层电子数可知,位于第IA族,故选B.
点评:本题考查元素周期表的结构与应用,为高频考点,把握质子数的计算及结构与性质的关系等为解答的关键,侧重分析与应用能力的考查,注意结构与位置的关系,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
反应4NH3(g)+5O2(g)=4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的速率可表示为( )
| A、v(NH3)=0.01 mol?L-1?s-1 |
| B、v(O2)=0.001 mol?L-1?s-1 |
| C、v(NO)=0.001 mol?L-1?s-1 |
| D、v(H2O)=0.045 mol?L-1?s-1 |
根据下列实验事实:①A+B2+═A2++B;②C+2H2O
C(OH)2+H2↑;③C2+的氧化性比A2+弱;④由B、D为电极组成的原电池,电极反应为:D2++2e-→D和B→B2++2e-.推断A、B、C、D的还原性由强到弱的顺序是( )
| ||
| A、C>A>B>D |
| B、C>D>A>B |
| C、A>C>B>D |
| D、C>B>A>D |
核磁共振(NMR)技术已广泛应用于复杂分子结构的测定和医学诊断等高科技领域.已知只有质子数或中子数为奇数的原子核有NMR现象.试判断下列哪种原子不能产生NMR现象( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列判断错误的是( )
| A、沸点:NH3>PH3>AsH3 |
| B、熔点:Li>Na>K |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
下列说法正确的是( )
A、按系统命名法, 的名称是2,3-二乙基丁烷 的名称是2,3-二乙基丁烷 |
B、某烃的衍生物A的分子式为C6H12O2,已知 ,又知D不与NaHCO3溶液反应,C和E都不能发生银镜反应,则A的结构可能有4种 ,又知D不与NaHCO3溶液反应,C和E都不能发生银镜反应,则A的结构可能有4种 |
| C、完全燃烧相同碳原子、且相同质量的烷烃、烯烃、炔烃,耗氧量最大的是烷烃 |
| D、已知烃A的分子式为C5Hm,烃B的最简式为C5Hn(m、n均为正整数),则烃A和烃B不可能互为同系物 |
 铝及其化合物用途广泛
铝及其化合物用途广泛