题目内容
4.下列判断错误的是( )| A. | 酸性:HClO4>H2SO4>H3PO4 | B. | 沸点:H2O<H2S<H2Se | ||
| C. | 碱性:NaOH>Mg(OH)2>Al(OH)3 | D. | 熔点:金刚石>NaCl>冰 |
分析 A.非金属性越强,最高价氧化物的水化物的酸性越强;
B.结构相似的分子晶体,相对分子质量越大,沸点越大,含有氢键的沸点较高;
C.金属性越强,最高价氧化物的水化物的碱性越强;
D.熔点为原子晶体>离子晶体>分子晶体.
解答 解:A.非金属性Cl>S>P,则最高价氧化物的水化物的酸性为HClO4>H2SO4>H3PO4,故A正确;
B.结构相似的分子晶体,相对分子质量越大,沸点越大,含有氢键的沸点较高,则沸点为H2S<H2Se<H2O,故B错误;
C.金属性Na>Mg>Al,则最高价氧化物的水化物的碱性为NaOH>Mg(OH)2>Al(OH)3,故C正确;
D.熔点为原子晶体>离子晶体>分子晶体,则熔点为SiO2(原子晶体)>NaCl(离子晶体)>SiI4(分子晶体),故D正确;
故选B.
点评 本题考查熔沸点的比较、非金属和金属性的比较,明确常见的比较的方法是解答本题的关键,注意知识的归纳整理,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
5.下列各组离子在水溶液中能大量共存的是( )
| A. | Na+、Ba2+、Cl-、SO42- | B. | Ca2+、HCO3-、Cl-、K+ | ||
| C. | Mg2+、Ag+、NO3-、Cl- | D. | H+、Cl-、Na+、CO32- | ||
| E. | SO32-、Ba2+,H+,NO3- |
15.下列各组物质能用分液漏斗分离的是( )
| A. | 苯和甲苯 | B. | 溴和溴苯 | C. | 水和己烷 | D. | 水和乙醛 |
19.心酮胺是治疗冠心病的药物,它具有如下结构简式.下列关于心酮胺的叙述错误的是( )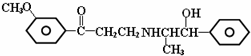
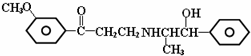
| A. | 可以发生加成反应 | B. | 可以发生消去反应 | ||
| C. | 可以发生银镜反应 | D. | 可以发生酯化反应 |
9.下列各种转化中,属于生物质能的化学转化的是( )
| A. | 石油燃烧 | |
| B. | 木材燃烧 | |
| C. | 在汽化炉内加热固体生物质,同时通入空气或水蒸气,或者隔绝空气高温加热生物质,使之发生复杂的化学反应产生可燃气体 | |
| D. | 杂草和人畜粪便加入沼气发酵池中生成沼气 |
16.下列两种有机物是某些药物中的有效成分:
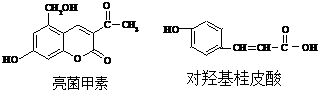
以下说法正确的是( )

以下说法正确的是( )
| A. | 将各1mol的两种物质分别与氢氧化钠溶液充分反应,消耗等量氢氧化钠 | |
| B. | 将各1mol的两种物质分别与溴水充分反应,消耗等量溴分子 | |
| C. | 将各1mol的两种物质分别与氢气充分反应,消耗等量氢气 | |
| D. | 两种有机物中的所有原子均不可能共平面 |
13.下列反应中,起固氮作用的是( )
| A. | NH3经催化氧化生成NO | B. | NO与O2反应生成NO2 | ||
| C. | N2与H2在一定条件下反应生成NH3 | D. | 由NH3制碳酸氢铵和硫酸铵 |
14.NOx是大气污染的主要污染物之一.
(1)硝酸厂常用如下三种方法处理氮氧化物(NO与NO2)尾气
①催化还原法:在催化剂存在时用H2将NO2还原为N2,
②Na2CO3溶液吸收法:用Na2CO3溶液吸收NO2生成CO2,若9.2g NO2和Na2CO3溶液完全反应时转移0.1mol电子,则反应的离子方程式为2NO2+CO32-=NO3-+NO2-+CO2.
③烧碱吸收法:氮氧化物(NO与NO2)用烧碱进行吸收,产物为NaNO2、NaNO3和H2O,现有含0.5mol氮氧化物的尾气,恰好被一定体积的25%NaOH溶液(密度1.28g/cm3)完全吸收.已知反应后溶液中含有0.35mo1NaNO2,若将尾气中NO与NO2的平均组成记为NOx,则x=1.8.
(2)现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体在标准状况下的体积与剩余固体的质量如表:
①稀硝酸的浓度为4mol•L-1
②计算原混合物中铁和铜的物质的量比为2:1;
③加入400mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为1.2mol.
(1)硝酸厂常用如下三种方法处理氮氧化物(NO与NO2)尾气
①催化还原法:在催化剂存在时用H2将NO2还原为N2,
②Na2CO3溶液吸收法:用Na2CO3溶液吸收NO2生成CO2,若9.2g NO2和Na2CO3溶液完全反应时转移0.1mol电子,则反应的离子方程式为2NO2+CO32-=NO3-+NO2-+CO2.
③烧碱吸收法:氮氧化物(NO与NO2)用烧碱进行吸收,产物为NaNO2、NaNO3和H2O,现有含0.5mol氮氧化物的尾气,恰好被一定体积的25%NaOH溶液(密度1.28g/cm3)完全吸收.已知反应后溶液中含有0.35mo1NaNO2,若将尾气中NO与NO2的平均组成记为NOx,则x=1.8.
(2)现将一定量的铁和铜的混合物分为等质量的4份,分别加入等浓度不同体积的稀硝酸(假设反应中稀硝酸的还原产物只有NO),产生气体在标准状况下的体积与剩余固体的质量如表:
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 | 8960mL |
②计算原混合物中铁和铜的物质的量比为2:1;
③加入400mL稀硝酸,反应完全后,溶液中硝酸根离子的物质的量为1.2mol.
