题目内容
17.有下列反应:①甲烷在空气中燃烧②丙烯使溴水褪色③由乙炔制聚氯乙烯塑料的单体 ④苯与浓硝酸、浓硫酸的混合酸反应⑤用重铬酸钾溶液检验酒驾 ⑥用异戊二烯合成橡胶其中属于氧化反应的是(填序号,下同)①⑤,属于取代反应的是④.
分析 ①甲烷在空气中燃烧,被氧化生成二氧化碳和水;
②丙烯含有碳碳双键,可溴水发生加成反应;
③乙炔与HCl发生加成反应可生成制聚氯乙烯塑料的单体;
④苯与浓硝酸、浓硫酸的混合酸反应为取代反应;
⑤用重铬酸钾溶液检验酒驾,乙醇被氧化;
⑥用异戊二烯合成橡胶,为加聚反应.
解答 解:①甲烷在空气中燃烧,被氧化生成二氧化碳和水,属于氧化还原反应;
②丙烯含有碳碳双键,可溴水发生加成反应;
③乙炔与HCl发生加成反应可生成制聚氯乙烯塑料的单体,属于加成反应;
④苯与浓硝酸、浓硫酸的混合酸反应生成硝基苯,为取代反应;
⑤用重铬酸钾溶液检验酒驾,乙醇被氧化;
⑥用异戊二烯合成橡胶,为加聚反应.
故答案为:①⑤;④.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物官能团与性质的关系为解答的关键,侧重常见有机物性质及反应类型的考查,题目难度不大.

练习册系列答案
相关题目
8.下列根据实验现象得出的结论正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 废FeCl3蚀刻液中加入少量铁粉、振荡 | 得到澄清溶液 | 蚀刻液中一定不含Cu2+ |
| B | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | 稀硫酸能氧化Fe2+ |
| C | KBrO3溶液中加入少量苯,然后通入少量Cl2,充分振荡,静置 | 有机相呈现橙色 | 氧化性:Cl2>Br2 |
| D | 葡萄糖溶液与新制Cu(OH)2混合加热 | 生成砖红色沉淀 | 葡萄糖分子中含有醛基 |
| A. | A | B. | B | C. | C | D. | D |
12.下列说法不正确的是( )
| A. | 甲苯与氢气完全加成后的产物的一氯代物有5种 | |
| B. | 分子式为C4H9Br的卤代烃 (不考虑立体异构)有4种 | |
| C. | 在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH | |
| D. | 用甘氨酸(H2N-CH2-COOH)和丙氨酸[CH3CH(NH2)COOH]脱水缩合最多可形成4种二肽 |
2.下列氧化物不能与铝粉发生铝热反应的是( )
| A. | Cr2O3 | B. | MnO2 | C. | WO3 | D. | MgO |
6.科学家研制多种新型杀虫剂代替DDT,化合物A是其中的一种,下列关于化合物A的说法正确的是( )

| A. | 可与FeCl3溶液发生显色反应 | |
| B. | 分子中最少有4个碳原子共平面 | |
| C. | 能发生取代反应和银镜反应 | |
| D. | 与H2完全加成的物质的量之比为1:1 |
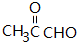 .
.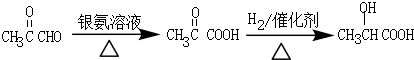 .
.