题目内容
NA为阿伏加德罗常数,下列叙述正确的是( )
A、 0.5mol雄黄(As4S4,已知As和N同主族,结构如图)含有NA个S-S键 |
| B、46g乙醇溶液中,所含的氧原子数为NA |
| C、1mol二氧化碳分子中共用电子对数为4NA |
| D、标准状况下,含NA个氩原子的氩气的体积约为11.2L |
考点:阿伏加德罗常数
专题:化学反应速率专题
分析:A、S是ⅥA族元素,可以形成2个化学键(H2S)、4个化学键(H2SO3)、6个化学键(H2SO4);As是ⅤA族元素,可以形成3个化学键、5个化学键,可以类比P,分析结构特征;
B、乙醇溶液中含有乙醇和水;
C、依据碳原子和氧原子结构结合二氧化碳分子结构分析判断;
D、氩气是单原子分子.
B、乙醇溶液中含有乙醇和水;
C、依据碳原子和氧原子结构结合二氧化碳分子结构分析判断;
D、氩气是单原子分子.
解答:
解:A、S是ⅥA族元素,可以形成2个化学键(H2S)、4个化学键(H2SO3)、6个化学键(H2SO4);As是ⅤA族元素,可以形成3个化学键、5个化学键,可以类比P,所以黑色的是S,白色的是As,故雄黄中不存在S-S键,故A错误;
B、乙醇溶液中含有的乙醇和水中 都含有氧元素,46g乙醇溶液中,所含的氧原子数大于NA,故B错误;
C、依据碳原子最外层电子数4个,形成四个共价键,氧原子结构是最外层电子数为6个,形成2个共价键,结合二氧化碳分子结构分析可知,1mol二氧化碳分子中共用电子对数为4NA,故C正确;
D、氩气是单原子分子,标准状况下,含NA个氩原子的氩气的体积约为22.4L,故D错误;
故选C.
B、乙醇溶液中含有的乙醇和水中 都含有氧元素,46g乙醇溶液中,所含的氧原子数大于NA,故B错误;
C、依据碳原子最外层电子数4个,形成四个共价键,氧原子结构是最外层电子数为6个,形成2个共价键,结合二氧化碳分子结构分析可知,1mol二氧化碳分子中共用电子对数为4NA,故C正确;
D、氩气是单原子分子,标准状况下,含NA个氩原子的氩气的体积约为22.4L,故D错误;
故选C.
点评:本题考查了物质结构的分析判断,掌握基础是关键,注意稀有气体是单原子分子,题目难度中等.

练习册系列答案
相关题目
柑橘中柠檬烯的结构可表示为 ,下列关于这种物质的说法中正确的是( )
,下列关于这种物质的说法中正确的是( )
 ,下列关于这种物质的说法中正确的是( )
,下列关于这种物质的说法中正确的是( )| A、与苯的结构相似,性质也相同 |
| B、所有原子可能共平面 |
| C、最多有18个原子共平面 |
| D、该物质极易溶于水 |
已知H2(g)+
O2(g)=H2O(g)△H=-241.8kJ/mol,下列说法中不正确的是( )
| 1 |
| 2 |
| A、2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol |
| B、1 mol H2完全燃烧生成液态水放出的热大于241.8kJ |
| C、断裂1mol H2O的化学键吸收的总能量大于断裂1 mol H2和0.5mol O2的化学键所吸收的总能量 |
| D、H2的燃烧热为241.8kJ/mol |
现有A、B、C、D四种金属片,进行如下的实验:①将A、B用金属导线连接后同时浸入稀硫酸中,A上有气泡产生;②C、D用金属导线连接后同时浸入稀硫酸中,电子流动的方向为:D→导线→C;③把A、D用金属导线连接后同时浸入稀硫酸中,D上发生还原反应.根据上述实验,四中金属的活动顺序正确的是( )
| A、A>B>C>D |
| B、C>B>A>D |
| C、B>A>D>C |
| D、D>C>A>B |
在空气中易被氧化的是( )
| A、Na2SO3 |
| B、盐酸 |
| C、浓硫酸 |
| D、稀硫酸 |
我“神舟七号”载人航天飞行任务实现了航天员的首次空间出舱活动.翟志刚等3位航天员在茫茫无际太空中迈出令中华儿女无比骄傲的一步.“神七”使用偏二甲肼(C2H8N2)和四氧化二氮作火箭燃料.则C2H8N2的同分异构体中不含有碳碳键的有几种( )
| A、2 种 |
| B、3 种 |
| C、5 种 |
| D、6种 |
在铜锌电池中,下列叙述正确的是( )
| A、正极附近硫酸根离子浓度增大 |
| B、负极附近硫酸根离子浓度减小 |
| C、正极附近硫酸根离子浓度减小 |
| D、若锌片、铜片同时有气泡冒出,说明锌不纯 |
对下列有机反应类型的认识中,不正确的是( )
A、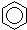 +HNO3 +HNO3
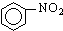 +H2O;取代反应 +H2O;取代反应 | |||
| B、CH4+Cl2→CH3Cl+HCl;置换反应 | |||
C、CH2═CH2+H2O
| |||
D、2CH3CH2OH+O2
|