题目内容
3.通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀.请回答.(1)用化学符号表示下列微粒:C:NH4+,D:OH-.
(2)写出A、B、E三种微粒反应的离子方程式:Al3++3NH3+3H2O=Al(OH)3↓+3NH4+或Mg2++2NH3+2H2O=Mg(OH)2↓+2NH4+.
分析 常见的10电子分子有H2O、NH3、CH4、HF等,常见的10电子阳离子有Na+、Mg2+、Al3+、NH4+、H3O+,常见的10电子阴离子有F-、OH-,根据“B溶于A后所得的物质可电离出C和D”,可推出A为H2O、B为NH3、C为NH4+、D为OH-,再根据A、B、E反应后可得C和一种白色沉淀,可推出E为Mg2+或Al3+,以此解答.
解答 解:常见的10电子分子有H2O、NH3、CH4、HF等,常见的10电子阳离子有Na+、Mg2+、Al3+、NH4+、H3O+,常见的10电子阴离子有F-、OH-,根据“B溶于A后所得的物质可电离出C和D”,可推出A为H2O、B为NH3、C为NH4+、D为OH-,再根据A、B、E反应后可得C和一种白色沉淀,可推出E为Mg2+或Al3+,
(1)由上述分析可知,C为NH4+,D为OH-,
故答案为:NH4+;OH-;
(2)A为H2O、B为NH3,E为Mg2+或Al3+,A、B、E三种微粒反应的离子方程式为:Al3++3NH3+3H2O═Al(OH)3↓+3NH4+或Mg2++2NH3+2H2O═Mg(OH)2↓+2NH4+;
故答案为:Al3++3NH3+3H2O=Al(OH)3↓+3 NH4+或Mg2++2NH3+2H2O=Mg(OH)2↓+2NH4+.
点评 本题考查无机物的推断、离子反应等,题目难度中等,掌握常见的10电子微粒及其性质是推断的关键,B溶于A后所得的物质可电离出C和D为解答的突破口.

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
14.正确认识官能团有助于了解有机物的性质,下列有关物质官能团的说法正确的是( )
| A. | 油脂分子中都含有碳碳双键 | B. | 葡萄糖分子中含有羟基和醛基 | ||
| C. | 水分子中含有羟基 | D. | 乙酸乙酯分子中含有羧基 |
13.2014年我国纪念“世界水日”活动的宣传主题为“加强河湖管理,建设水生态文明”.下列与水相关的叙述正确的是( )
| A. | 加聚反应也可能有水生成 | |
| B. | 水、乙醇、氢氧化钠中都存在羟基 | |
| C. | 水可以参与有些有机反应,有些有机反应也有水生成 | |
| D. | 有水参加的有机化学反应都可以叫做水解反应 |
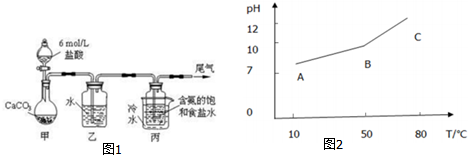
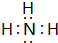 .
. 已知:A、B、C、D、E、F六种元素核电荷数依次增大,属于周期表中前四周期的元素.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满.请根据以上信息,回答下列问题:
已知:A、B、C、D、E、F六种元素核电荷数依次增大,属于周期表中前四周期的元素.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的熔点在同周期元素形成的单质中是最高的;F原子核外最外层电子数与B相同,其余各层均充满.请根据以上信息,回答下列问题: