题目内容
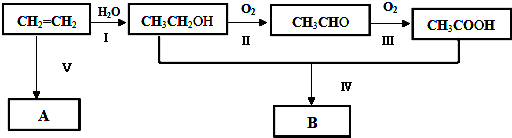
2.2015年6月5日是世界环境日,今年的主题是“践行绿色生活,”下列有关说法中错误的是( )| A. | 煤的气化、液化是使煤变成清洁能源,减少环境污染的有效途径 | |
| B. | 高纯硅可制作太阳能电池,二氧化硅可制作光导纤维 | |
| C. | 利用工业生产产生的二氧化碳制造全降解塑料,可以缓解温室效应 | |
| D. | 棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O |
分析 A.煤的气化、液化能去除硫等杂质;
B.高纯硅是常用的半导体材料,二氧化硅晶体有导光性;
C.温室效应是由二氧化碳的大量排放造成的;
D.羊毛的主要成分是蛋白质,含有氮元素.
解答 解:A.煤的气化、液化可以除掉煤中的S等杂质,能减少有害气体二氧化硫的排放,故A正确;
B.高纯硅是常用的半导体材料,是制造太阳能电池的重要材料,二氧化硅晶体有导光性,可制作光导纤维,故B正确;
C.利用工业生产产生的二氧化碳制造全降解塑料,可以减少二氧化碳的排放,能缓解温室效应,故C正确;
D.羊毛的主要成分是蛋白质,含有氮元素,燃烧生成生成N2、CO2和H2O,故D错误;
故选D.
点评 本题考查清洁能源、蛋白质的成分、硅单质和二氧化硅的用途、温室效应等,注意煤的气化、液化可以除掉煤中的杂质,使煤变成清洁能源,题目比较简单.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 离子化合物中一定含有金属阳离子 | |
| B. | 离子化合物中只含有离子键 | |
| C. | 在酸碱盐中,碱与盐一定属于离子化合物 | |
| D. | 离子键一定存在于化合物中 |
10.下表是元素周期表的一部分,针对表中的①~⑦种元素,填写下列空白:
(1)在这些元素中,(用元素符号填写,下同)金属性最强的元素是Na;非金属性最强的是Cl;最不活泼的元素是Ar.
(2)这些元素的最高价氧化物的对应水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是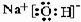 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.
(3)②的氢化物分子式为NH3,属于共价化合物(填“共价”或“离子”);
(4)⑤元素的原子结构示意图为 .
.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ |
(2)这些元素的最高价氧化物的对应水化物中,酸性最强的化合物的分子式是HClO4;碱性最强的化合物的电子式是
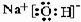 ;能形成两性氢氧化物的元素是Al.
;能形成两性氢氧化物的元素是Al.(3)②的氢化物分子式为NH3,属于共价化合物(填“共价”或“离子”);
(4)⑤元素的原子结构示意图为
 .
.
17.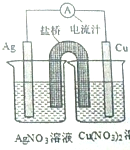 某同学用铜片,银片,Cu(NO3)2溶液,AgNO3溶液,导线和盐桥(装有琼脂-KN03的U形管)设计一个原电池如图所示,下列判断中正确的是( )
某同学用铜片,银片,Cu(NO3)2溶液,AgNO3溶液,导线和盐桥(装有琼脂-KN03的U形管)设计一个原电池如图所示,下列判断中正确的是( )
 某同学用铜片,银片,Cu(NO3)2溶液,AgNO3溶液,导线和盐桥(装有琼脂-KN03的U形管)设计一个原电池如图所示,下列判断中正确的是( )
某同学用铜片,银片,Cu(NO3)2溶液,AgNO3溶液,导线和盐桥(装有琼脂-KN03的U形管)设计一个原电池如图所示,下列判断中正确的是( )| A. | 实验过程中,左右两侧烧杯中,NO3-浓度变化情况分别为不变,增大 | |
| B. | 实验过程中,取出盐桥,该原电池也能继续工作 | |
| C. | 若开始使用U形铜管代替盐桥,装置中有电流产生,铜管质量不变 | |
| D. | 若开始时用U形铜管代替盐桥,装置中无电流产生 |
7.下列各组物质中,互为同系物的是( )
| A. | CH4和CH3CH2CH3 | B. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | ||
| C. | 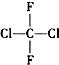 和 和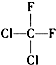 | D. |  和CH3-CH2-CH2-CH3 和CH3-CH2-CH2-CH3 |
11.对于放热反应H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl,下列说法正确的是( )
| A. | 该反应涉及到离子键和共价键的断裂与形成 | |
| B. | 该反应中,化学能只转变为热能 | |
| C. | 断开1molH-H键和1molCl-Cl键所吸收的总能量,小于形成1molH-Cl键所放出的能量 | |
| D. | 反应物所具有的总能量高于产物所具有的总能量 |
12.下列氧化反应属于吸热反应的是( )
| A. | 二氧化碳与赤热的炭反应生成一氧化碳 | |
| B. | 葡萄糖在人体内氧化分解 | |
| C. | 锌粒与稀H2SO4反应制取H2 | |
| D. | Ba(OH)2•8H2O与NH4Cl反应 |