题目内容
某校高一化学研究性学习小组对日常生活中的氯气用途进行了调查,了解到氯气可广泛地应用于衣物的漂白、水体的杀菌和消毒等.
(1)氯气可以用于漂白、消毒的原因是因为能与水作用形成具有 性的次氯酸,相关反应的离子方程式为 ;
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5mg/L至1.0mg/L之间时,效果最好.图是该小组测定的每天19:00时泳池中水的氯含量,哪几天使用泳池不安全 ;

(3)你认为哪几天的天气炎热、阳光强烈 ,说出一种理由是 ;
(4)在对泳池水中通入氯气消毒时,当发生氯气泄漏时,应立即关闭氯气罐,还应采取下列自救方法 .(选填序号)
A、用湿润的毛巾捂住口鼻跑向低处
B、用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处
C、用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处
D、用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
(5)小型泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液而非氯气的一项理由 ;
(6)请再写出你能知道的能用于饮用水消毒的消毒剂(至少写三种,否则不得分)
请在你书写的药品中选择一种你认为最好的带上飞机,并说明它的原因.选择 原因 .
(1)氯气可以用于漂白、消毒的原因是因为能与水作用形成具有
(2)在调查某室外游泳池夏季池水消毒情况时,小组成员了解到,该游泳池每周一上午8:00换水,然后通入氯气消毒,通常游泳池水的含氯量控制在0.5mg/L至1.0mg/L之间时,效果最好.图是该小组测定的每天19:00时泳池中水的氯含量,哪几天使用泳池不安全

(3)你认为哪几天的天气炎热、阳光强烈
(4)在对泳池水中通入氯气消毒时,当发生氯气泄漏时,应立即关闭氯气罐,还应采取下列自救方法
A、用湿润的毛巾捂住口鼻跑向低处
B、用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处
C、用浸湿浓氨水的毛巾捂住口鼻匍匐跑至安全处
D、用浸湿食盐水的毛巾捂住口鼻顺风跑至安全处
(5)小型泳池通常使用漂白液(NaClO溶液)而非氯气来消毒池水,试举出使用漂白液而非氯气的一项理由
(6)请再写出你能知道的能用于饮用水消毒的消毒剂(至少写三种,否则不得分)
请在你书写的药品中选择一种你认为最好的带上飞机,并说明它的原因.选择
考点:氯气的化学性质,氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:(1)氯气与水反应生成盐酸、次氯酸,次氯酸具有漂白性;
(2)游泳池水的含氯量控制在0.5mg/L至1.0mg/L之间时,效果最好,根据图中提供的信息可以进行相关方面的判断;
(3)HClO不稳定;
(4)氯气的密度比空气大,能够显碱性的物质发生化学反应;
(5)从保存和运输的角度分析;
(6)漂白粉、二氧化氯、双氧水、过氧乙酸、臭氧及高铁酸钠等物质都可以用于饮用水消毒的消毒剂.
(2)游泳池水的含氯量控制在0.5mg/L至1.0mg/L之间时,效果最好,根据图中提供的信息可以进行相关方面的判断;
(3)HClO不稳定;
(4)氯气的密度比空气大,能够显碱性的物质发生化学反应;
(5)从保存和运输的角度分析;
(6)漂白粉、二氧化氯、双氧水、过氧乙酸、臭氧及高铁酸钠等物质都可以用于饮用水消毒的消毒剂.
解答:
解:(1)氯气可以用于漂白、消毒的原因是因为能与水作用形成具有强氧化性的次氯酸,发生的离子反应为Cl2+H2O═H++Cl-+HClO,
故答案为:强氧化;Cl2+H2O═H++Cl-+HClO;
(2)由图中可知,星期六、星期日的含氯量控制在0.5mg/L以下,是不安全的,故答案为:星期六、星期日;
(3)因为阳光强烈时HClO更易分解,致含氯量下降明显,所以导致星期四到星期六的含氯量下降明显,故答案为:星期四到星期六;阳光强烈时HClO更易分解,致含氯量下降明显;
(4)氯气的密度比空气大,能够显碱性的物质发生化学反应,所以应该用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处,氨水碱性较强,具有刺激性气味,食盐水不能吸收氯气,故答案为:B;
(5)通常使用漂白液(NaClO溶液)而非氯气来消毒池水的原因是:NaClO更稳定,便于储存和运输,故答案为:NaClO更稳定,便于储存和运输;
(6)能用于饮用水消毒的消毒剂有:漂白粉、二氧化氯、双氧水、过氧乙酸、臭氧及高铁酸钠等;最好带漂白粉上飞机,因为漂白粉具有强氧化性,具有杀菌消毒作用,比其他药品易于存放运输,且安全,
故答案为:漂白粉;这种物质具有强氧化性,具有杀菌消毒作用,比其他药品易于存放运输,且安全.
故答案为:强氧化;Cl2+H2O═H++Cl-+HClO;
(2)由图中可知,星期六、星期日的含氯量控制在0.5mg/L以下,是不安全的,故答案为:星期六、星期日;
(3)因为阳光强烈时HClO更易分解,致含氯量下降明显,所以导致星期四到星期六的含氯量下降明显,故答案为:星期四到星期六;阳光强烈时HClO更易分解,致含氯量下降明显;
(4)氯气的密度比空气大,能够显碱性的物质发生化学反应,所以应该用浸湿小苏打或肥皂水的毛巾捂住口鼻跑向高处,氨水碱性较强,具有刺激性气味,食盐水不能吸收氯气,故答案为:B;
(5)通常使用漂白液(NaClO溶液)而非氯气来消毒池水的原因是:NaClO更稳定,便于储存和运输,故答案为:NaClO更稳定,便于储存和运输;
(6)能用于饮用水消毒的消毒剂有:漂白粉、二氧化氯、双氧水、过氧乙酸、臭氧及高铁酸钠等;最好带漂白粉上飞机,因为漂白粉具有强氧化性,具有杀菌消毒作用,比其他药品易于存放运输,且安全,
故答案为:漂白粉;这种物质具有强氧化性,具有杀菌消毒作用,比其他药品易于存放运输,且安全.
点评:本题考查氯气的化学性质,为高频考点,把握发生的反应及物质的性质为解答的关键,侧重分析能力及知识综合应用能力的考查,注意图中信息和化学知识有机地结合起来进行分析、判断,从而得出正确的结论,题目难度中等.

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目
下列与实验相关的叙述正确的是( )
| A、用苯萃取溴水中的Br2时,有机层从分液漏斗的下端放出 |
| B、检验溶液中是否含有SO42-,依次滴入Ba(NO3)2溶液和稀盐酸 |
| C、配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余溶液吸出 |
| D、配制AlCl3溶液时,将AlCl3溶解在较浓的盐酸中,再用水稀释到所需浓度 |
设NA为阿伏加德罗常数,下列说法中不正确的是( )
| A、2.3g金属钠变为钠离子时失去的电子数是0.1NA |
| B、0.5NA个氯分子所占体积约为11.2L |
| C、28g氮气所含原子数为2NA |
| D、18g水所含的质子总数为10NA |

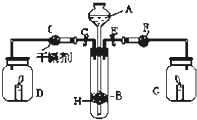 为证明有关物质的性质,某学生设计了如图所示的装置.当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛熄灭;关闭C 打开E时,则看到G中蜡烛燃得更亮,且F中盛放固体为淡黄色.
为证明有关物质的性质,某学生设计了如图所示的装置.当打开活塞C,使液体A与隔板H上的固体B相遇时,即有气体产生,并发现D中蜡烛熄灭;关闭C 打开E时,则看到G中蜡烛燃得更亮,且F中盛放固体为淡黄色.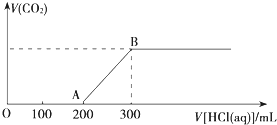 向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.
向100mL 3mol?L-1的NaOH溶液中缓慢通入一定量的CO2,充分反应,测得最后溶液的pH>7.