题目内容
向(1)根据计算确定金属氧化物的名称。
(2)计算通电后硫酸溶液的物质的量浓度(溶液体积按100 mL计算)。
解析:(1)设该二价金属的摩尔质量为M,根据电子守恒定律:![]() ×4,M=
×4,M=
(2)通电过程中,阴极上每生成1 mol Cu,阳极上OH-放电消耗2 mol OH-,同时生成2 mol H+,n(H+)=![]() ×2=0.04 mol。
×2=0.04 mol。
c(H2SO4)=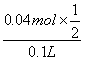 =0.2 mol·L-1。
=0.2 mol·L-1。
答案:(1)氧化铜 (2)0.2 mol·L-1

练习册系列答案
相关题目