题目内容
18.电子层数相同的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性由强到弱顺序为:HXO4>H2YO4>H3ZO4,下列判断错误的是( )| A. | 原子半径 X>Y>Z | B. | 气态氢化物稳定性X>Y>Z | ||
| C. | 元素原子得电子能力X>Y>Z | D. | 单质与氢气反应难易X>Y>Z |
分析 电子层数相同的三种元素X、Y、Z位于同一周期,同周期元素从左到右元素的非金属性逐渐增强,对应的最高价氧化物对应水化物的酸性逐渐增强,酸性相对强弱:HXO4>H2YO4>H3ZO4,可知非金属性X>Y>Z,原子序数X>Y>Z,再结合元素周期律解答.
解答 解:电子层数相同的三种元素X、Y、Z位于同一周期,同周期元素从左到右元素的非金属性逐渐增强,对应的最高价氧化物对应水化物的酸性逐渐增强,酸性相对强弱:HXO4>H2YO4>H3ZO4,可知非金属性X>Y>Z,原子序数X>Y>Z.
A.同周期自左而右原子半径减小,故原子半径:X<Y<Z,故A错误;
B.非金属性越强,氢化物越稳定,由于非金属性X>Y>Z,所以气态氢化物的稳定性:X>Y>Z,故B正确;
C.非金属性越强,得电子能力越强,则元素原子得电子能力由强到弱X>Y>Z,故C正确;
D.非金属性X>Y>Z,非金属性越强,单质与氢气反应越容易,故D正确,
故选A.
点评 本题考查元素周期律知识,题目难度不大,注意相关性质的比较角度以及元素周期律的主要递变规律,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
8.化合物X的分子式为C5H11Cl,用NaOH的醇溶液处理X,可得分子式为C5H10的两种产物Y、Z,Y、Z经催化加氢后都可得到2-甲基丁烷.若将化合物X用NaOH的水溶液处理,则所得有机产物的结构简式可能是( )
| A. | CH3CH2CH2CH2CH2OH | B. | 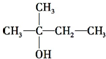 | ||
| C. | 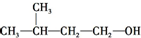 | D. | 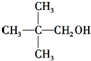 |
9.下列各组有机化合物中,肯定属于同系物的一组是( )
| A. | C3H6与C5H10 | B. | C3H8与C5H12 | C. | C2H6O与C5H8O | D. | C7H8与C6H6 |
6.下列化学反应属于加成反应的是( )
| A. | CH4+Cl2$\stackrel{光}{→}$CH3Cl+HCl | |
| B. | CH2═CH2+HCl$\stackrel{催化剂}{→}$CH3CH2Cl | |
| C. | CH3COOC2H5+H2O$?_{△}^{H+}$CH3COOH+C2H5OH | |
| D. | CH2═CH2+H2$→_{△}^{Ni}$CH2CH3 |
13.检验氨气可以用( )
| A. | 湿润的红色石蕊试纸 | B. | 干燥的红色石蕊试纸 | ||
| C. | 干燥的蓝色石蕊试纸 | D. | 湿润的蓝色石蕊试纸 |
7.排布在下列各电子层上的一个电子,所具有的能量最低的是( )
| A. | K层 | B. | L层 | C. | M层 | D. | N层 |
8.向1L、0.4mol/LH2SO4溶液中加入10.1gKNO3和9.6g铜粉,充分反应后产生的气体在标准状况下的体积为( )
| A. | 2.24L | B. | 3.36L | C. | 4.48L | D. | 5.60L |