题目内容
将SO2气体通入H2S水溶液中直至过量,下列表示溶液pH随SO2气体体积变化关系示意图正确的是( )
A、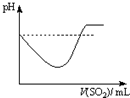 |
B、 |
C、 |
D、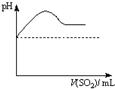 |
考点:弱电解质在水溶液中的电离平衡
专题:
分析:H2S为酸,其溶液呈酸性,pH<7,通入二氧化硫后发生反应SO2+2H2S=3S↓+2H2O,导致溶液酸性减弱,pH增大,当二氧化硫过量时溶液变为亚硫酸溶液,亚硫酸的酸性大于氯化氢,据此分析解答.
解答:
解:将SO2气体通入H2S水溶液中直至过量,发生的反应为:SO2+2H2S=3S↓+2H2O,随着反应进行,溶液酸性减弱,PH增大;当SO2过量时,SO2+H2O=H2SO3,反应生成亚硫酸,溶液酸性增强,所以PH又减小,由于亚硫酸酸性大于硫化氢的酸性,故后来的PH比最初要小,
故选C.
故选C.
点评:本题考查了溶液pH变化,明确酸的强弱及物质的性质是解本题关键,根据溶液中的溶质及其性质确定溶液pH变化,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KmnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
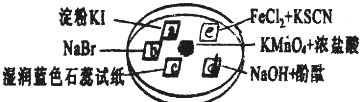
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,对实验的“解释或结论”正确的是( )

已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,对实验的“解释或结论”正确的是( )
| A、a、b两处均有颜色变化,证明单质氧化性:CI2>Br2>I2 |
| B、c处先变红,后褪色,证明氯气与水反应生成了酸性物质 |
| C、d处立即褪色,证明氯气与水反应生成了漂白性物质 |
| D、e处变红色,证明氧化性:C12>Fe3+,还原性:Cl-<Fe2+ |
下列离子方程式书写正确的为( )
A、石灰石与盐酸反应:C
| ||
| B、醋酸与烧碱溶液反应:H++OH-═H2O | ||
| C、氧化铜与盐酸反应:O2-+2H+═H2O | ||
| D、硫酸与氨水混合:H++NH3?H2O═NH4++H2O |
关于含阳离子O2+的化合物O2AsF6,下列叙述中错误的是( )
| A、O2+共有11个核外电子 |
| B、化合物中含有离子键、极性共价键、非极性共价键 |
| C、化合物O2ASF6中AS的化合价为+5价 |
| D、化合物O2ASF6为离子化合物 |
化学与科学、技术、社会和环境密切相关.下列有关说法中错误的是( )
| A、对废旧电池进行回收处理,主要是为了环境保护和变废为宝 |
| B、用电解水的方法制取大量H2,可以缓解能源不足的问题 |
| C、大力开发和应用氢能源有利于实现“低碳经济” |
| D、工业上,不能采用电解MgCl2溶液的方法制取金属镁 |
下列物质属于纯净物的是( )
| A、福尔马林 | B、冰醋酸 |
| C、汽油 | D、聚丙烯酸甲酯 |
下列反应中属于氧化还原反应的是( )
| A、SO3+H2O=H2SO4 | ||||
| B、CaCO3+2HCl=CaCl2+H2O+CO2↑ | ||||
| C、Cl2+H2O=HCl+HClO | ||||
D、2NaHCO3
|