题目内容
如图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸.向KmnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面.
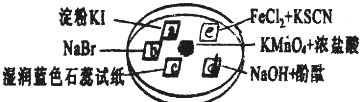
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,对实验的“解释或结论”正确的是( )

已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O,对实验的“解释或结论”正确的是( )
| A、a、b两处均有颜色变化,证明单质氧化性:CI2>Br2>I2 |
| B、c处先变红,后褪色,证明氯气与水反应生成了酸性物质 |
| C、d处立即褪色,证明氯气与水反应生成了漂白性物质 |
| D、e处变红色,证明氧化性:C12>Fe3+,还原性:Cl-<Fe2+ |
考点:氧化性、还原性强弱的比较
专题:氧化还原反应专题
分析:A、Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变红棕色,可证明氧化性:Cl2>I2、Cl2>Br2;
B、c处先变红,说明氯气与水生成酸性物质,后褪色,则证明氯气与水生成具有漂白性物质;
C、d处立即褪色,也可能是氯气与水生成酸性物质中和了NaOH;
D、e处变红说明Cl2将Fe2+氧化为Fe3+,证明还原性:Fe2+>Cl-,反应的离子方程式2Fe2++Cl2═2Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3;用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-═2FeO42-+3Cl-+5H2O.
B、c处先变红,说明氯气与水生成酸性物质,后褪色,则证明氯气与水生成具有漂白性物质;
C、d处立即褪色,也可能是氯气与水生成酸性物质中和了NaOH;
D、e处变红说明Cl2将Fe2+氧化为Fe3+,证明还原性:Fe2+>Cl-,反应的离子方程式2Fe2++Cl2═2Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3;用FeCl3与KClO在强碱性条件下反应制取K2FeO4,反应的离子方程式为2Fe3++3ClO-+10OH-═2FeO42-+3Cl-+5H2O.
解答:
解:A、Cl2分别与KI、NaBr作用生成I2、Br2,a处变蓝、b处变橙色,可证明氧化性:Cl2>I2、Cl2>Br2,无法证明I2与Br2之间氧化性的强弱,故A错误;
B、氯气与水反应Cl2+H2O═H++Cl-+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则c处先变红,后褪色,能证明氯气与水生成了酸性物质和漂白性物质,故B错误;
C、Cl2和氢氧化钠反应生成氯化钠、次氯酸钠和水,消耗了氢氧化钠红色退去,不能证明生成物质具有漂白性,故C错误;
D、Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2═2Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3,证明还原性Fe2+>Cl-,故D正确.
故选:D.
B、氯气与水反应Cl2+H2O═H++Cl-+HClO,H+使试纸变红,HClO具有漂白性,可使试纸褪色,则c处先变红,后褪色,能证明氯气与水生成了酸性物质和漂白性物质,故B错误;
C、Cl2和氢氧化钠反应生成氯化钠、次氯酸钠和水,消耗了氢氧化钠红色退去,不能证明生成物质具有漂白性,故C错误;
D、Cl2将Fe2+氧化为Fe3+,试纸变为红色,反应的离子方程式2Fe2++Cl2═2Fe3++2Cl-;Fe3++3SCN-═Fe(SCN)3,证明还原性Fe2+>Cl-,故D正确.
故选:D.
点评:本题通过元素化合物知识,考查考生实验能力和对实验现象的分析、推断能力,题目难度中等,注意把握氯气以及其它物质的相关化学性质,把握离子检验方法和特征反应的现象是关键.

练习册系列答案
相关题目
下列说法正确的是( )
| A、离子化合物中可能含有共价键,但不一定含有金属元素 |
| B、分子中一定含有共价键 |
| C、非极性分子中一定存在非极性键 |
| D、对于组成结构相似的分子,一定是相对分子质量越大,熔沸点越高 |
因为自然界的水含有很多杂质,要经过一定处理措施后才能饮用.下列处理过程中没有发生了物理变化的是( )
| A、过滤悬浮物质 |
| B、投药品,消毒杀菌 |
| C、用活性炭吸附杂质 |
| D、制成蒸馏水 |
一定条件下反应2AB(g)?A2(g)+B2(g)达到平衡状态的标志是( )
| A、AB的消耗速率等于A2的消耗速率 |
| B、容器中气体的密度不随时间变化 |
| C、容器内,3种气体AB、A2、B2共存 |
| D、容器中各组分的体积分数不随时间变化 |
“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥缩聚反应 ⑦酯化反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤加聚反应 ⑥缩聚反应 ⑦酯化反应.
| A、②⑤ | B、④⑤ | C、⑥⑦ | D、①③ |
下列各组中的两种物质相互作用时,反应条件或反应物的用量改变,对生成物没有影响的是( )
| A、过氧化钠和二氧化碳 |
| B、钠和氧气 |
| C、氢氧化钠和二氧化碳 |
| D、碳和氧气 |
下列离子方程式书写正确的是( )
| A、氢氧化钠溶液加到稀硫酸中:OH-+H+═H2O |
| B、金属钠投入到水中:Na+H2O═Na++OH-+H2↑ |
| C、石灰石投入到稀盐酸中:CO32-+2H+═CO2↑+H2O |
| D、Fe粉加入稀盐酸中:2Fe+6H+═Fe3++3H2↑ |
下列过程是非自发的是( )
| A、水由高处向低处流 |
| B、室温下,水结成冰 |
| C、气体从高密度处向低密度处扩散 |
| D、盐酸与氢氧化钠溶液反应 |