题目内容
4.已知14.2g气体G在标准状况下的体积是4.48L,则气体G的摩尔质量是( )| A. | 28.4 | B. | 28.4g/mol | C. | 71 | D. | 71g/mol |
分析 根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$计算.
解答 解:根据n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$可知:M=$\frac{m•{V}_{m}}{V}$=$\frac{14.2g•22.4L/mol}{4.48L}$=71g/mol.
故选D.
点评 本题考查了摩尔质量的概念和计算方法,注意摩尔质量是由单位的,单位为g/mol,要求学生熟练掌握物质的量与气体摩尔体积、阿伏伽德罗常数、摩尔质量、物质的量浓度等之间的转化关系,试题培养了所学灵活应用所学知识解决实际问题的能力,题目难度不大.

练习册系列答案
相关题目
12.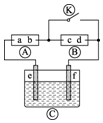 如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通
如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述不正确的是( )
后,使c、d两点短路.下列叙述不正确的是( )
 如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通
如图为直流电源,?为浸透饱和碘化钾溶液和淀粉溶液的滤纸,?为电镀槽.接通电路后发现?上的d点显蓝色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述不正确的是( )
后,使c、d两点短路.下列叙述不正确的是( )| A. | f电极为锌板 | B. | c极发生的反应为2H++2e-═H2↑ | ||
| C. | a为直流电源的正极 | D. | e极发生氧化反应 |
13.下列反应的离子方程式正确的是( )
| A. | 用氨水溶解氯化银沉淀:Ag++2NH3•H2O=[Ag(NH3)2]++2H2O | |
| B. | Mg(HCO3)2溶液中加入足量NaOH溶液:Mg2++2HCO3-+2OH-═Mg CO3↓+CO32-+2H2O | |
| C. | Na2O2固体投入H218O中:2H218O+2Na2O2=4Na++4OH-+18O2↑ | |
| D. | 苯酚钠溶液跟AlCl3溶液反应:3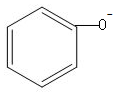 +Al3++3H2O→ +Al3++3H2O→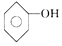 +Al(OH)3↓ +Al(OH)3↓ |
12.根据实验操作和现象所得出的结论正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 向NaAlO2溶液中滴入NaHCO3溶液 | 有白色沉淀生成 | AlO2-结合H+的能力比CO32-强 |
| B | 向某溶液中滴入氯水,再滴加KSCN溶液 | 溶液显血红色 | 原溶液中一定有Fe2+ |
| C | 向某无色溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中一定无NH4+ |
| D | 用洁净的铂丝蘸取某溶液进行焰色反应 | 火焰呈黄色 | 原溶液中一定有Na+、无K+ |
| A. | A | B. | B | C. | C | D. | D |
9.下列各组物质中,每一种物质都能使氯水褪色的是( )
| A. | AgNO3溶液、CCl4、BaCl2溶液 | B. | Na2SO3溶液、FeCl3溶液、H2S溶液 | ||
| C. | SO2气体、KOH溶液、镁粉 | D. | NaOH溶液、CO气体、石蕊溶液 |
14.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.1mol Cu与足量的浓硫酸完全反应后,溶液中Cu2+数目为0.1NA | |
| B. | 标准状况下,11 g由3H和16O组成的超重水中,电子数和中子数均为5NA | |
| C. | 标准状况下,将3.36L Cl2通入1 L0.2 mol•L-1的FeBr2溶液中,被氧化的Br-数目为0.1NA | |
| D. | 等物质的量过氧化钠和氧化纳固体中所含阴离子数均为NA |