题目内容
18.下列微粒中,与NH4+的电子总数和质子总数都相同的是( )| A. | Na+ | B. | F | C. | OH- | D. | CH4 |
分析 根据微粒中质子数为各原子的质子数之和,若微粒为分子,质子数=电子数;若微粒为阳离子,电子数=质子数-电荷数;若微粒为阴离子,电子数=质子数+电荷数;
解答 解:由于N的质子数为7,H的质子数为1,所以NH4+中质子数为11,电子数为10个,
A、Na+中质子数为11,电子数为10,故A符合;
B、F中质子数为9,电子数为9个,故B不符合;
C、OH-中质子数为9,电子数为10,故C不符合;
D、CH4中质子数为10,电子数为10,故D不符合.
故选A.
点评 本题考查微粒质子数、电子数的相互关系,难度较小,关键理解质子数与电子数关系确定微粒电性.

练习册系列答案
相关题目
6.已知短周期元素的离子aW3+、bX+、cY2-、dZ-具有相同的电子层结构,则下列叙述正确的是( )
| A. | 还原性:Z->Y2- | B. | 原子半径:W>X>Y>Z | ||
| C. | 离子半径:Y2->Z->X+>W3+ | D. | 原子序数d>c>b>a |
3.下列离子在溶液中能大量共存的是( )
| A. | H+、Fe2+、ClO-、Na+ | B. | Na+、H+、SO42-、CO32- | ||
| C. | Fe3+、Cl-、Br-、SCN- | D. | Al3+、NO3-、H+、NH4+ |
10.短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素.其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外),W、Z之间与W、Q之间原子序数之差相等,五种元素原子最外层电子数之和为21.下列说法不正确的是( )
| A. | 气态氢化物的稳定性:Y>X>W | |
| B. | Y与Q的氢化物相遇生成白烟 | |
| C. | 气态氢化物的还原性:W>X>Y | |
| D. | Q可分别与X、Y、Z、W形成化学键类型相同的化合物 |
7.下列各组物质,属于同分异构体的是( )
| A. | 正丁烷与异丁烷 | B. | 白磷和红磷 | ||
| C. | ${\;}_{1}^{1}$H2和${\;}_{1}^{2}$H2 | D. | H2O与H2O2 |
8.下列实验方法或操作正确的是( )
| A. |  萃取碘水中碘 | B. |  给液体加热 | C. |  干燥NH3 | D. |  制取淡水 |
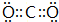 ,B与D形成的原子个数比为1:1的化合物乙的电子式是
,B与D形成的原子个数比为1:1的化合物乙的电子式是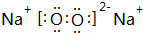 .
.