题目内容
(共8分)
某无色溶液,其中可能存在Na+、Ba2+、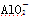 、S2-、
、S2-、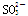 、
、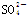 。取该溶液进行有关实验,实验结果如图所示。
。取该溶液进行有关实验,实验结果如图所示。
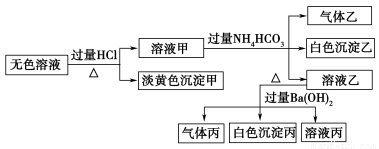
请回答下列问题:
(1)沉淀甲的化学式为________ ,白色沉淀乙的化学式为________
(2)由溶液甲生成沉淀乙的离子方程式为__________________ 。
(3)沉淀丙中一定含有_________(填化学式,下同),可能含有_______________。
(4)综合上述信息,该溶液中肯定存在的离子有_____________ 。
(1)S (1分) Al(OH)3 (1分)
(2)Al3++ ===Al(OH)3↓+3CO2↑ (2分)
===Al(OH)3↓+3CO2↑ (2分)
(3)BaCO3 BaSO4 (2分)
(4)S2-、 、
、 、Na+(共2分,少写给1分,多写不给分)
、Na+(共2分,少写给1分,多写不给分)
【解析】
试题分析:沉淀甲的颜色是淡黄色,所以该沉淀应是S单质,说明该溶液中存在S2-、 ,二者在酸性条件下发生氧化还原反应生成S单质;所以该溶液中一定不含Ba2+,一定含有Na+,再加入过量碳酸氢铵后有沉淀产生,说明该溶液中一定含有
,二者在酸性条件下发生氧化还原反应生成S单质;所以该溶液中一定不含Ba2+,一定含有Na+,再加入过量碳酸氢铵后有沉淀产生,说明该溶液中一定含有 ,过量的盐酸使
,过量的盐酸使 以铝离子形式存在,铝离子与碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,所以沉淀乙是氢氧化铝,气体乙是二氧化碳。溶液乙中含有过量的碳酸氢铵、氯化钠、氯化铵,所以加入过量的氢氧化钡溶液,有气体丙生成,则气体丙是氨气,碳酸氢根离子与氢氧化钡反应生成碳酸钡沉淀,所以生成的沉淀一定含有碳酸钡,可能含有硫酸钡,硫酸根离子不能确定。
以铝离子形式存在,铝离子与碳酸氢根离子发生双水解反应生成氢氧化铝沉淀和二氧化碳气体,所以沉淀乙是氢氧化铝,气体乙是二氧化碳。溶液乙中含有过量的碳酸氢铵、氯化钠、氯化铵,所以加入过量的氢氧化钡溶液,有气体丙生成,则气体丙是氨气,碳酸氢根离子与氢氧化钡反应生成碳酸钡沉淀,所以生成的沉淀一定含有碳酸钡,可能含有硫酸钡,硫酸根离子不能确定。
(1)根据以上分析沉淀甲的化学式为S;白色沉淀乙的化学式为Al(OH)3;
(2)溶液甲中含有铝离子,与碳酸氢根离子发生双水解反应,离子方程式为Al3++ ==Al(OH)3↓+3CO2↑;
==Al(OH)3↓+3CO2↑;
(3)沉淀丙中一定含有BaCO3,可能含有BaSO4;
(4)根据以上分析溶液中一定存在的离子是S2-、 、
、 、Na+。
、Na+。
考点:考查溶液中离子的判断,离子方程式的书写

无色溶液中含有:①Na+、②Ba2+、③C1—、④Br—、⑤SO32-、⑥SO42-、⑦Fe2+离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
步骤 | 操作 | 现象 |
① | 用pH试纸检验 | 溶液的pH大于7 |
② | 向溶液中滴加氯水,再加入CC14振荡,静置 | CC14层呈橙红色 |
③ | 取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
根据上述实验现象,判断以下结论中正确的是
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑤⑦
C.可能含有的离子是①②⑥ D.不能确定的离子是①③⑥
 C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变。
C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变。