题目内容
(12分)某物质M具有硬度大、熔沸点高、高温下电绝缘性好、无毒等优良性能。经检测M中只含有两种短周期元素。现取82 gM溶于适量的NaOH溶液中恰好完全反应,得到无色溶液A和44.8 L气体B(气体体积为标准状况下测定),该气体能使湿润的红色石蕊试纸变蓝。往无色溶液A中逐滴加入盐酸,可观察到溶液先变浑浊后变澄清。请回答下列问题:
(1)物质M的化学式为 ,属于 晶体(填“分子”、“离子”或“原子”)。
(2) 写出M与NaOH反应的化学方程式
(3)工业碱性废水中若含有NO2-,可用铝粉除去。已知此反应产物中检测到B气体。写出上述反应的
离子方程式 。若改用电解法将废水中NO2-转换为N2除去,N2将在 (填“阴极”或“阳
极”)生成。
(4)C12与B以3︰1的物质的量之比反应生成HCl和一种二元化合物X(该反应中只有一种元素化合价改变)。X大量应用于面粉的漂白和消毒,写出X与水反应的化学方程式
(12分)
(1)AlN(2分) 原子(2分)
(2)AlN+ H2O +NaOH==NaAlO2 + NH3 (2分)
(3)2Al+NO2-+OH-+H2O==2AlO2- + NH3↑(2分)阴(2分)
(4)NCl3+3H2O=NH3↑+3HClO (2分)
【解析】
试题分析:M中只含有两种短周期元素,现取82gM溶于适量的NaOH溶液中恰好反应,得到无色溶液A和44.8L气体B(气体体积为标准状况下),该气体能使红色石蕊试纸变蓝,则气体B是NH3,故M中含有氮元素,氨气的物质的量为2mol,则M中氮元素质量=2mol×14g/mol=28g,另外一种元素的质量=82g-28g=54g;往反应后的溶液中逐滴加入盐酸,可观察到溶液先变浑浊后变澄清,则反应后的溶液中溶质A是NaAlO2,故M含有Al元素,其物质的量=54g÷27g/mol=2mol,M中Al与N原子物质的量之比为2mol:2mol=1:1,故M是AlN。
(1)由上述分析,可知物质M的化学式为AlN,具有硬度大、熔沸点高、高温下电绝缘性好,应属于原子晶体。
(2)AlN与NaOH反应的化学方程式为:AlN+NaOH+H2O=NaAlO2+NH3↑。
(3)工业碱性废水中若含有NO2-,可用铝粉除去.此反应产物中检测到NH3气体,还应生成偏铝酸根,反应离子反应方程式为2Al+NO2-+OH-+H2O=2AlO2-+NH3↑;若改用电解法将废水中NO-2转换为N2除去,亚硝酸根得电子生成氮气,发生还原反应,所以应该在阴极上生成。
(4)C12与NH3以3:1的物质的量之比反应生成HCl和一种二元化合物X(该反应中只有一种元素化合价改变),则只能是Cl元素化合价变化,故X为NCl3,X大量应用于面粉的漂白和消毒,与水反应的方程式为:NCl3+3H2O=NH3↑+3HClO。
考点:本题考查无机物推断、方程式的书写、电解原理、晶体类型的判断。

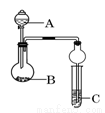
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项 | 现象或事实 | 解 释 |
A | 用浸泡酸性高锰酸钾溶液的硅土延长果实的成熟 | 利用乙烯可以发生加成反应
|
B | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
C | SO2能使品红溶液褪色 | SO2具有还原性 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |
 NaAlO2(aq)
NaAlO2(aq) Al(OH)3 ②S
Al(OH)3 ②S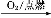 SO3
SO3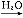 H2SO4
H2SO4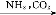 NaHCO3
NaHCO3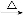 Na2CO3
Na2CO3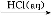 FeCl3(aq)
FeCl3(aq)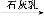 Mg(OH)2
Mg(OH)2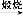 MgO
MgO
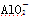 、S2-、
、S2-、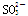 、
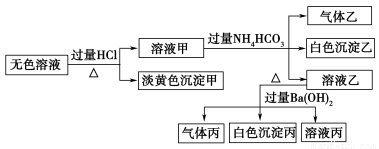
、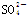 。取该溶液进行有关实验,实验结果如图所示。
。取该溶液进行有关实验,实验结果如图所示。