题目内容
设NA代表阿伏加德罗常数,下列说法不正确的是( )
| A、醋酸的摩尔质量与NA个醋酸分子的质量在数值上相等 |
| B、NA个氧原子和NA个氢分子的质量比为8:1 |
| C、标准状况下,22.4L 乙醇(CH3CHOOH)中含有的氧原子数为2.0NA |
| D、在常温常压下,0.5NA个氯气分子所占体积大于11.2L |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.摩尔质量以g/mol为单位时,在数值上摩尔质量与粒子的相对原子量或相对分子量相等;
B.NA个氧原子和NA个氢分子的物质的量都是1mol,1mol氧原子的质量为16g,1mol氢分子的质量为2g;
C.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算乙醇的物质的量;
D.常温下,气体摩尔体积大于22.4L/mol.
B.NA个氧原子和NA个氢分子的物质的量都是1mol,1mol氧原子的质量为16g,1mol氢分子的质量为2g;
C.标准状况下,乙醇的状态不是气体,不能使用标况下的气体摩尔体积计算乙醇的物质的量;
D.常温下,气体摩尔体积大于22.4L/mol.
解答:
解:A.醋酸的摩尔质量为60g/mol,NA个醋酸分子的质量为60g,二者在数值上相等,故A正确;
B.NA个氧原子的物质的量为1mol,质量为8g,NA个氢分子的质量为2g,二者的质量比为:16g:2g=8:1,故B正确;
C.标准状况下,乙醇为液体,题中条件无法计算22.4L 乙醇的物质的量,故C错误;
D.标况下气体摩尔体积为22.4L/mol,常温下的气体摩尔体积大于22.4L/mol,0.5NA个氯气分子的物质的量为0.5mol,所占体积大于11.2L,故D正确;
故选C.
B.NA个氧原子的物质的量为1mol,质量为8g,NA个氢分子的质量为2g,二者的质量比为:16g:2g=8:1,故B正确;
C.标准状况下,乙醇为液体,题中条件无法计算22.4L 乙醇的物质的量,故C错误;
D.标况下气体摩尔体积为22.4L/mol,常温下的气体摩尔体积大于22.4L/mol,0.5NA个氯气分子的物质的量为0.5mol,所占体积大于11.2L,故D正确;
故选C.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确乙醇在标况下为液体,要求掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项A为易错点,注意摩尔质量的单位可能为kg/mol.

练习册系列答案
相关题目
设NA代表阿伏加德罗常数,下列说法正确的是( )
| A、22.4L O2中含有NA个氧分子 |
| B、2.4g金属镁变成镁离子时失去的电子数目为0.1NA |
| C、18g H2O所含电子数目为10NA |
| D、在25℃,压强为1.01×105Pa时,11.2L氮气所含的原子数目为NA |
与反应Cl2+SO2+2H2O=H2SO4+2HCl中水的作用完全相同的是( )
A、2H2O
| ||||
| B、Cl2+H2O=HCl+HClO | ||||
C、3Fe+4H2O(g)
| ||||
| D、2Na+2H2O=2NaOH+H2↑ |
应用元素周期律的有关知识,可以预测我们不知道的一些元素及其化合物的性质.下列预测中不正确的是
( )
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液作用,均产生氢气
③At单质为有色固体,At难溶于水易溶于四氯化碳
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥H2Se是无色、有毒,比H2S稳定的气体.
( )
①Be的氧化物的水化物可能具有两性
②Tl能与盐酸和NaOH溶液作用,均产生氢气
③At单质为有色固体,At难溶于水易溶于四氯化碳
④Li在氧气中剧烈燃烧,产物是Li2O2,其溶液是一种强碱
⑤SrSO4是难溶于水的白色固体
⑥H2Se是无色、有毒,比H2S稳定的气体.
| A、①②③④ | B、②④⑥ |
| C、①③⑤ | D、②④⑤ |
Q、W、X、Y、Z是原子序数依次增大的短周期元素,X的焰色反应呈黄色.Q元素的原子最外层电子数是其内层电子数的2倍.W、Z最外层电子数相同,Z的核电荷数是W的2倍.元素Y的合金是日常生活中常用的金属材料.下列说法正确的是( )
| A、原子半径的大小顺序:rX>rY>rW>rQ |
| B、元素Q和Z能形成QZ2型的共价化合物 |
| C、X、Y的最高价氧化物的水化物之间不能反应 |
| D、工业上常用电解的方法制备X、Y的单质 |
下列装置中(杯中均盛海水)铁腐蚀最快的是( )
A、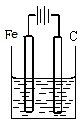 |
B、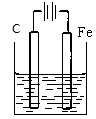 |
C、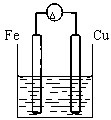 |
D、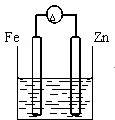 |
天宫一号搭载的长征二号火箭使用的主要燃料是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4=3N2+4H2O+2CO2,下列叙述错误的
是( )
是( )
| A、此反应中R的分子式为C2H8N2 |
| B、此反应是氧化还原反应,N2O4做氧化剂 |
| C、每生成67.2L N2转移电子数为8NA |
| D、此反应可在瞬间产生大量高温气体,推动火箭飞行 |
下列有关氨的性质的叙述中正确的是( )
①氨不能在空气中燃烧②氨水呈碱性③氨气和酸相遇都能产生白色烟④在反应:NH3+H+═NH4+中氨失去电子被氧化⑤氨水中含氮微粒中最多的是NH4+.
①氨不能在空气中燃烧②氨水呈碱性③氨气和酸相遇都能产生白色烟④在反应:NH3+H+═NH4+中氨失去电子被氧化⑤氨水中含氮微粒中最多的是NH4+.
| A、①② | B、③⑤ | C、①⑤ | D、②⑤ |
已知相同条件下,HClO的电离常数小于H2CO3的第一级电离常数(Ka1)大于H2CO3的第二级电离常数(Ka2).为了提高氯水中HClO的浓度,可行的是( )
| A、通入HCl(g) |
| B、加入NaHCO3(s) |
| C、加入H2O |
| D、加入NaOH(s) |