题目内容
10.现有S2-、SO32-、NH4+、Al3+、HPO42-、Na+、SO42-、AlO2-、Fe3+、HCO3-、Cl-等离子,请按要求填空:(1)在水溶液中,该离子水解呈碱性的是S2-、SO32-、HPO42-、AlO2-、HCO3-;
(2)在水溶液中,该离子水解呈酸性的是NH4+、Al3+、Fe3+;
(3)既能在酸性较强的溶液里大量存在,又能在碱性较强的溶液里大量存在的离子有Na+、SO42-、Cl-;
(4)既不能在酸性较强的溶液里大量存在,又不能在碱性较强的溶液里大量存在的离子有HPO42-、HCO3-.
分析 (1)弱酸根离子水解显碱性;
(2)弱碱离子水解显碱性;
(3)与氢离子、氢氧根离子均不反应的离子,可大量共存;
(4)与酸、碱均反应的离子,为酸式酸根离子,不能大量存在.
解答 解:(1)S2-、SO32-、HPO42-、AlO2-、HCO3-属于弱酸根离子,水解显碱性,故答案为:S2-、SO32-、HPO42-、AlO2-、HCO3-;
(2)NH4+、Al3+、Fe3+均属于弱碱阳离子,水解显酸性,故答案为:NH4+、Al3+、Fe3+;
(3)既能在酸性较强溶液里、又能在碱性较强的溶液里大量存在的离子,是和氢离子、氢氧根离子都不反应的离子,强酸的酸根离子和强碱的阳离子,为Na+、SO42-、Cl-,故答案为:Na+、SO42-、Cl-.
(4)与酸、碱均反应的离子,为酸式酸根离子,不能大量存在,为HPO42-、HCO3-,故答案为:HPO42-、HCO3-.
点评 本题考查盐类水解及离子共存,为高频考点,把握盐类水解原理及常见离子之间的反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
5.下列表示对应化学反应的离子方程式正确的是( )
| A. | 铜与硝酸银溶液反应:Cu+Ag+═Cu2++Ag | |
| B. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O | |
| C. | 向Ca(ClO)2溶液中通入二氧化硫:Ca2++2ClO-+SO2+H2O═CaSO3↓+2HClO | |
| D. | 氯化钙溶液中通入二氧化碳气体:Ca2++CO2+H2O═CaCO3↓+2H+ |
15.下列反应的离子方程式书写正确的是( )
| A. | 胃舒平(主要含氢氧化铝)治疗胃酸过多:OH-+H+═H2O | |
| B. | 醋酸除水垢:2H++CaCO3═Ca2++H2O+CO2↑ | |
| C. | 敞口的澄清石灰水变质:Ca2++2OH-+2CO2═Ca(HCO3)2 | |
| D. | 稀盐酸除铁锈:6H++Fe2O3═2Fe3++3H2O |
19.下列能形成原电池的装置(溶液均为稀硫酸)是( )
| A. |  | B. | 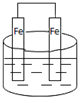 | C. |  | D. |  |
20.下列反应属于离子反应和氧化还原反应,同时溶液颜色又发生变化的是( )
| A. | BaCl2溶液与K2SO4溶液反应 | B. | Cl2通入NaOH溶液中 | ||
| C. | NaOH溶液与CuSO4溶液反应 | D. | Cl2通入NaI溶液中 |
