题目内容
4.酸性KMnO4、H2O2在生产、生活、卫生医疗中常用作消毒剂,其中H2O2可用于漂白,是化学实验室里必备的重要氧化试剂.高锰酸钾造成的污渍可用还原性的草酸(H2C2O4)去除,Fe(NO3)3也是重要氧化试剂,请按要求回答下到问题.
(1)在酸往条件下KMnO4的氧化性会增强.用来酸化KMnO4溶液的最佳试剂是b.
a.硝酸 b.硫酸 c.盐酸
(2)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,写出该反应的化学方程式Cu+H2O2+2HCl=CuCl2+2H2O.
分析 (1)硝酸具有强氧化性,盐酸能被高锰酸钾氧化,而高锰酸钾与硫酸不反应;
(2)反应生成氯化铜、水.
解答 解:(1)硝酸具有强氧化性,盐酸能被高锰酸钾氧化,而高锰酸钾与硫酸不反应,则用来酸化KMnO4溶液的最佳试剂是硫酸,故答案为:b;
(2)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,该反应的化学方程式为Cu+H2O2+2HCl=CuCl2+2H2O,故答案为:Cu+H2O2+2HCl=CuCl2+2H2O.
点评 本题考查氧化还原反应,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意氧化还原反应遵循电子守恒,题目难度不大.

练习册系列答案
相关题目
14.澄清透明的溶液中,下列离子组中能大量共存的是( )
| A. | Cu2+、Na+、OH- | B. | H+、Cl-、CH3COO- | C. | Fe2+、H+、NO3- | D. | K+、Ca2+、NO3- |
19.下列微粒: 其核外电子数相同的是( )
其核外电子数相同的是( )
 其核外电子数相同的是( )
其核外电子数相同的是( )| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
9.将2mol A气体和1mol B气体在固定体积的密闭容器中混合并在一定条件下发生如下反应并达到平衡状态:2A(g)+B(g)?2C(g),此反应为放热反应.下列能增大正、逆反应速率的方法是:
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
(1)再充入1mol A气体;(2)充入2mol的惰性气体;(3)加入正催化剂;(4)升高温度;(5)移走部分C气体.
其中正确的是( )
| A. | (1)(3)(5) | B. | (1)(3)(4) | C. | (1)(2)(4)(5) | D. | (1)(2)(3)(4)(5) |
8.下列对于NH3和CO2的说法中正确的是( )
| A. | 都是直线形结构 | |
| B. | 中心原子都采取sp1杂化 | |
| C. | NH3为三角锥形结构,CO2为直线形结构 | |
| D. | 氮原子和碳原子上都没有孤对电子 |
9.下列有关物质用途的说法错误的是( )
| A. | 过氧化钠可用作潜艇里氧气的来源 | B. | 二氧化硅是制造光电池的原料 | ||
| C. | 氯气可用于制造漂白粉 | D. | 硅酸钠溶液可用作木材防火剂 |
 仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去).请按要求回答:
仔细阅读图,已知B、D、E、F、G是氧化物,其中D是形成酸雨的主要污染物,F、K是氢化物,且F在常温下为液态;C、H是日常生活中最为常见的金属单质,J是气态非金属单质,O是白色沉淀,且B、H、L、M、N、O中含有同种元素(图中部分反应物或产物已略去).请按要求回答: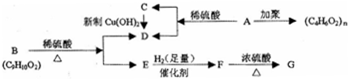
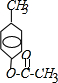 ;
;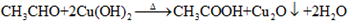 ,反应类型氧化反应;F→G
,反应类型氧化反应;F→G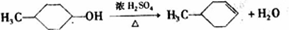 ,反应类型消去反应.
,反应类型消去反应.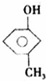 、
、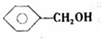 .
.