题目内容
下列有关物质的性质和该性质的应用均正确的是( )
| A、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓外壳的腐蚀 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| D、常温下浓硫酸能使铝发生钝化,可在常温下用铝制容器贮藏贮运浓硫酸 |
考点:铜金属及其重要化合物的主要性质,氯、溴、碘及其化合物的综合应用,浓硫酸的性质,硅和二氧化硅
专题:元素及其化合物
分析:A、根据牺牲阳极的阴极保护法来保护金属;
B、根据二氧化硅与氢氟酸反应来分析;
C、根据二氧化氯具有强氧化性而能用于杀菌消毒来分析;
D、根据浓硫酸的特性可知,常温下浓硫酸使铝钝化,生成一层致密的保护膜阻止反应进一步进行;
B、根据二氧化硅与氢氟酸反应来分析;
C、根据二氧化氯具有强氧化性而能用于杀菌消毒来分析;
D、根据浓硫酸的特性可知,常温下浓硫酸使铝钝化,生成一层致密的保护膜阻止反应进一步进行;
解答:
解:A、因要减缓船体的腐蚀应连接比铁更活泼的金属,如锌,这就是牺牲阳极的阴极保护法,故A错误;
B、因二氧化硅能与氢氟酸反应:SiO2 +4HF═SiF4↑+2H2O,所以不能用石英制造耐酸容器,故B错误;
C、因二氧化氯可用于自来水的杀菌消毒是因为其具有强氧化性,而不是还原性,故C错误;
D、因浓硫酸具有强氧化性,能够与大多数金属反应,但遇到金属铝、铁要发生钝化,因此常温下用铝、铁制贮罐贮运浓硫酸,故D正确;
故选D.
B、因二氧化硅能与氢氟酸反应:SiO2 +4HF═SiF4↑+2H2O,所以不能用石英制造耐酸容器,故B错误;
C、因二氧化氯可用于自来水的杀菌消毒是因为其具有强氧化性,而不是还原性,故C错误;
D、因浓硫酸具有强氧化性,能够与大多数金属反应,但遇到金属铝、铁要发生钝化,因此常温下用铝、铁制贮罐贮运浓硫酸,故D正确;
故选D.
点评:本题主要考查了物质的性质以及用途,题目较简单,试题具有一定的综合性.

练习册系列答案
相关题目
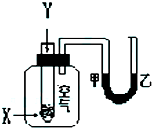 某学生用如图所示装置进行化学反应X+2Y═2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到U型管中液面甲处降乙处升.关于该反应的下列叙述:
某学生用如图所示装置进行化学反应X+2Y═2Z能量变化情况的研究.当往试管中滴加试剂Y时,看到U型管中液面甲处降乙处升.关于该反应的下列叙述:①该反应为放热反应;
②生成物的总能量比反应物更高;
③该反应过程可以看成是“贮存”于X、Y内部的能量转化为热量而释放出来.其中正确的是( )
| A、①②③ | B、②③ | C、①② | D、①③ |
下列有关煤和石油的叙述中错误的是( )
| A、煤是由有机物和无机物组成的复杂的混合物 |
| B、煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
| C、石油的催化裂化的目的主要是为了提高轻质油的产量和质量 |
| D、石油的裂解的目的主要是为了获取气态短链不饱和烃 |
下列说法错误的是( )
| A、石油中含有C5-C11的烷烃,可以通过石油的分馏得到汽油 |
| B、含C18以上的烷烃的重油经过催化剂裂化可以得到汽油 |
| C、石油的分馏、煤的干馏都是物理变化 |
| D、煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来 |
图中E表示反应物或生成物的能量,下列说法正确的是( )


| A、图1可表示C+O2→CO2的能量变化过程 |
| B、图1可表示CaCO3→CaO+CO2的能量变化过程 |
| C、图2可表示Mg+2HCl→MgCl2+H2 的能量变化过程 |
| D、图1表示的反应是吸热反应,图2表示的反应是放热反应 |

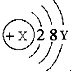 ,试回答:
,试回答: