题目内容
关于NaHCO3的性质,下列说法正确的是( )
| A、和酸反应放出等量的CO2所消耗的酸比Na2CO3少 |
| B、相同温度下溶解度比Na2CO3要大 |
| C、热稳定性比Na2CO3强 |
| D、NaHCO3只能和酸作用不能和碱作用 |
考点:钠的重要化合物
专题:元素及其化合物
分析:碳酸氢钠不稳定,加热易分解,可与酸反应生成二氧化碳,可与碱反应生成碳酸盐,以此解答该题.
解答:
解:A.分别滴加HCl溶液,反应离子方程式为CO32-+2H+═CO2↑+H2O,HCO3-+H+═H2O+CO2↑,则和酸反应放出等量的CO2所消耗的酸比Na2CO3少,故A正确;
B.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出,可知常温时水溶解性:Na2CO3>NaHCO3,故B错误;
C.NaHCO3不稳定,加热易分解:2NaHCO3
Na2CO3+CO2↑+H2O,碳酸钠受热稳定,故C错误;
D.NaHCO3可与酸反应生成二氧化碳气体,如与盐酸反应生成二氧化碳、氯化钠和水,也可与碱反应,如与氢氧化钠反应生成碳酸钠和水,故D错误.
故选A.
B.常温下,向饱和碳酸钠溶液中通入二氧化碳气体,有碳酸氢钠晶体析出,可知常温时水溶解性:Na2CO3>NaHCO3,故B错误;
C.NaHCO3不稳定,加热易分解:2NaHCO3
| ||
D.NaHCO3可与酸反应生成二氧化碳气体,如与盐酸反应生成二氧化碳、氯化钠和水,也可与碱反应,如与氢氧化钠反应生成碳酸钠和水,故D错误.
故选A.
点评:本题考查Na2CO3和NaHCO3性质的异同,注意相同条件下,可溶性碳酸盐的溶解度大于相应的碳酸氢盐,为易错点,注意把握Na2CO3和NaHCO3性质,题目难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
下列叙述中正确的是( )
| A、NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂 |
| B、工业上制H2SO4过程中SO2氧化条件一般选择高温、高压、催化剂 |
| C、浓H2SO4有强氧化性,常温下能与Cu发生反应 |
| D、将C12通入冷的消石灰中可制得漂白粉 |
四氯化硅结构和四氯化碳类似,对其性质判断①四氯化硅是分子晶体;②常温下为液态;③四氯化硅沸点较低;其中正确的是( )
| A、只有① | B、①③ |
| C、②③ | D、①②③ |
下列图示与对应的叙述相符合的是( )
A、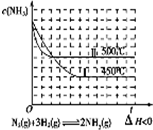 |
B、 |
C、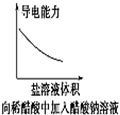 |
D、 |
下列说法或表示方法正确的是( )
| A、反应物总能量低于生成物总能量时,该反应不能发生 |
| B、在101 kPa,25℃时,2 g H2完全燃烧生成液态水,放出285.8 kJ的热量;氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l);△H=-285.8 kJ/mol |
| C、甲烷是清洁、无污染的化石燃料 |
| D、氢气是热值高、无污染的燃料 |
已知1-20号元素的离子:aW2+、bX+、CY2-、dZ- 具有相同的电子层结构,下列关系正确的是( )
| A、离子半径:aW2+>bX+>dZ->CY2- |
| B、b=c+3 |
| C、Z元素的非金属性比Y的强,HZ沸点一定比H2Y的高 |
| D、上述四种元素的最高价氧化物水化物都能与Al(OH)3反应生成盐和水 |
下列有关光合作用的说法不正确的是( )
| A、将无机物转化为有机物 |
| B、反应物的总能量高于生成物的总能量 |
| C、将太阳能转化为化学能 |
| D、是自然界碳元素循环的重要途径 |
室温下,下列各组离子在指定溶液中能大量共存的是( )
| A、(NH4)2Fe(SO4)2溶液中:Ba2+、K+、OH-、Br- | ||||
B、c(I-)=0.1 mol?L-1的溶液中:Na+、Fe3+、ClO-、S
| ||||
C、c(OH-)/c(H+)=10-12的溶液中:N
| ||||
D、新制饱和氯水中:Na+、Al3+、S
|