题目内容
室温下,在实验室中电解500mL某0.03mol/L的NaCl溶液,通电一段时间后溶液的pH从7增加到12时(设电解时溶液的体积变化忽略不计),则两极产生气体的总体积(标准状况)和溶液中NaCl的浓度分别为( )
| A、112mL,0.04mol/L |
| B、56mL,0.02mol/L |
| C、56mL,0.04mol/L |
| D、112mL,0.02mol/L |
考点:电解原理
专题:电化学专题
分析:电解饱和食盐水时,阳极上是氯离子失电子,电极反应为:2Cl--2e-═Cl2↑,阴极上是氢离子得电子,2H++2e-═H2↑,根据pH计算出溶液中的氢氧根离子、氢离子的浓度,然后计算气体的总体积以及溶液中NaCl的浓度.
解答:
解:电解饱和食盐水时,阳极上是氯离子失电子,电极反应为:2Cl--2e-═Cl2↑,阴极上是氢离子得电子,2H++2e-═H2↑,通电一段时间后溶液的pH从7增加到12时,则阴极上减少的氢离子浓度是0.01mol/L,物质的量是0.01mol/L×0.5L=0.005mol,转移电子是0.005mol,产生氢气和氯气各0.0025mol,总物质的量是0.005mol,标况下的体积是:0.005mol×22.4L/mol=0.112L=112mL,
反应的氯离子的物质的量是0.005mol,500mL0.03mol/L的NaCl溶液剩余的物质的量为:0.5L×0.03mol/L-0.005mol=0.01mol,浓度是
=0.02mol/L,
故选D.
反应的氯离子的物质的量是0.005mol,500mL0.03mol/L的NaCl溶液剩余的物质的量为:0.5L×0.03mol/L-0.005mol=0.01mol,浓度是
| 0.01mol |
| 0.5L |
故选D.
点评:本题考查学生电解池的工作原理以及电极反应式的书写和电子守恒的计算知识,注意知识的归纳和整理是关键,难度中等.

练习册系列答案
相关题目
下列叙述正确的是( )
| A、1个乙醇分子中存在8个π键 |
| B、NH3分子中心原子的杂化方式为SP2 |
| C、H2S和CS2分子都是含极性键的非极性分子 |
| D、PCl3和CCl4分子中所有原子的最外层都达到8电子稳定结构 |
下列各组物质间反应可能包括多步反应,其总的离子方程式正确的是( )
| A、等体积、等物质的量浓度的明矾溶液和Ba(OH)2溶液混合:3Ba2++6OH -+2Al3++3SO42-═2Al(OH)3↓+3BaSO4↓ |
| B、FeCl2在空气中被氧化:4Fe2++O2+2H2O═4Fe3++4OH - |
| C、AlCl3(aq)中投入过量Na:2Al3++6Na+6H2O═2Al(OH)3↓+6Na++3H2↑ |
| D、4molFeBr2 (aq) 中通入3molCl2:2Fe2++4Br-+3Cl2═2Fe3++2 Br2+6Cl- |
对于氯化铁溶液和氢氧化铁胶体,以下说法正确的是( )
| A、分散质粒子直径都在1nm~100nm之间 |
| B、分散质微粒都能透过半透膜 |
| C、加热蒸干并灼烧后都有氧化铁生成 |
| D、分散系中分散质微粒前者带电荷、后者不带电荷 |
下列物质的分类组合正确的是( )
| A | B | C | D | |
| 化合物 | CH3Cl | NaHSO4 | FeSO4?7H2O | KAl(SO4)2 |
| 氧化物 | H2O | NO | Al2O3 | Na2O |
| 电解质 | 盐酸 | 氨水 | 铁 | 烧碱 |
| 胶体[jtj | 酒精水溶液 | 豆浆 | 有色玻璃 | 云、雾 |
| A、A | B、B | C、C | D、D |
鉴别K2CO3和KHCO3两种白色固体,有4位同学为鉴别它们,分别设计了下列四种不同的方法,其中可行的是( )
| A、分别加入1 mol?L-1的盐酸溶液,看有无气泡产生 |
| B、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
| C、分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀 |
| D、分别配成溶液,用洁净铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色(可使用蓝色钴玻璃) |
有a L乙炔和乙烯的混合气体,在催化剂存在下与足量的H2发生加成反应,消耗H2 1.25a L,乙烯和乙炔的体积比为( )
| A、1:1 | B、2:1 |
| C、3:1 | D、4:1 |
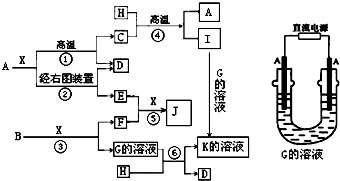 如图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液.请按要求填空:
如图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液.请按要求填空: