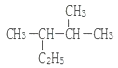题目内容
【题目】设NA代表阿伏加德罗常数的值。下列说法正确的是
A.2.4 g Mg与足量硝酸反应生成NO和![]() 的混合气体,失去的电子数为
的混合气体,失去的电子数为![]()
B.1 mol甲苯分子中所含单键数目为![]()
C.![]() 的
的![]() 溶液中,由水电离出的H+数目一定是
溶液中,由水电离出的H+数目一定是![]()
D.![]() 、
、![]() 和
和![]() 的混合气体中所含分子数为
的混合气体中所含分子数为![]()
【答案】D
【解析】
本题考查阿伏加德罗常数,意在考查对化学键,水的电离及物质性质的理解能力。
A.2.4g Mg与足量硝酸反应,Mg变为Mg2+,失去0.2mol电子,故A错误;
B.甲苯分子中含有9个单键(8个C-H键、1个C-C键),故B错误;
C.未指明温度,Kw无法确定,无法计算水电离的氢离子数目,故C错误;
D.CO2、N2O和C3H8的摩尔质量相同,均为44g/mol,故混合气体的物质的量为![]() =0.1 mol,所含分子数为0.1NA,故D正确;
=0.1 mol,所含分子数为0.1NA,故D正确;
答案:D

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】(1)下面是4种粒子的结构示意图:
A. B.
B. C.
C. D.
D.
图中粒子共能表示______种元素,图中表示的阳离子是_______(用离子符号表示),图中C所表示的元素在元素周期表中的位置______。
(2)在1-18号的短周期主族元素中,表中的字母代表一种元素,回答下列问题:
C | D | ||||||||
A | B | E | F |
①D单质的电子式为:______;
②F的最高价氧化物对应水化物的化学式为:______;
③E和F分别形成的气态氢化物中稳定性较弱是______;(填写氢化物的化学式)
④A最高价氧化物的水化物所含化学键为_______,其水溶液与B的最高价氧化物的水化物反应的离子方程式为__。