题目内容
恒温、恒压下,a molA和b molB在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成n molC.则下列说法中正确的是( )
| A、物质A、B的转化率之比为a:b |
| B、起始时刻和达平衡后容器中的压强比为(a+b):(a+b-n) |
| C、若起始时放入a molA、b molB、a mol氦气,则达平衡时生成小于n molC |
| D、当v正(A)=2v逆(B)时,可确定反应达平衡 |
考点:化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:反应 A(g)+2B(g)?2C(g),
开始 a b 0
转化0.5n n n
平衡a-0.5n b-n n
结合等效平衡及pV=nRT来解答.
开始 a b 0
转化0.5n n n
平衡a-0.5n b-n n
结合等效平衡及pV=nRT来解答.
解答:
解:A.由B可知,物质A、B的转化率之比为
:
=b:2a,故A错误;
B.恒温、恒压下,开始和平衡后的压强之比为为物质的量之比:(a+b):(a+b-0.5n),故B错误;
C.amolA和bmolB在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成nmolC;恒温、恒压下,起始时放入amolA和bmolB,起始量与原起始量成正比,二者为等效平衡,相当于加入a mol氦气,恒温、恒压下体积增大,压强减小,平衡逆向进行,所以平衡时C的浓度小于nmol,故C正确;
D.反应速率之比等于化学计量数之比,所以当2v正(A)=v逆(B)时,证明v逆(C)=v正(C)可断定反应应达平衡,v正(A)=2v逆(B),不能说明反应达到平衡状态,故D错误;
故选:C.
| 0.5n |
| a |
| n |
| b |
B.恒温、恒压下,开始和平衡后的压强之比为为物质的量之比:(a+b):(a+b-0.5n),故B错误;
C.amolA和bmolB在一个容积可变的容器中发生如下反应:A(g)+2B(g)?2C(g),一段时间后达到平衡,生成nmolC;恒温、恒压下,起始时放入amolA和bmolB,起始量与原起始量成正比,二者为等效平衡,相当于加入a mol氦气,恒温、恒压下体积增大,压强减小,平衡逆向进行,所以平衡时C的浓度小于nmol,故C正确;
D.反应速率之比等于化学计量数之比,所以当2v正(A)=v逆(B)时,证明v逆(C)=v正(C)可断定反应应达平衡,v正(A)=2v逆(B),不能说明反应达到平衡状态,故D错误;
故选:C.
点评:本题考查了化学平衡的转化率计算应用,速率之比等于系数之比是正反应速率之比,注意恒压容器反应前后压强相同,题目难度中等.

练习册系列答案
相关题目
下列化学反应的有机产物中,存在同分异构体的是( )
| A、(CH3)2CHCH2Br在碱性溶液中水解 |
| B、苯在催化剂FeCl3作用下与Cl2反应 |
C、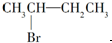 与NaOH的醇溶液共热反应 与NaOH的醇溶液共热反应 |
D、 在催化剂存在下与H2完全加成 在催化剂存在下与H2完全加成 |
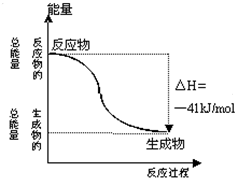 已知一定条件下,CO(g)+H2O (g)=CO2(g)+H2(g)反应过程能量变化如图所示,下列有关该反应的说法正确的是( )
已知一定条件下,CO(g)+H2O (g)=CO2(g)+H2(g)反应过程能量变化如图所示,下列有关该反应的说法正确的是( )| A、该反应为吸热反应 |
| B、CO(g)与H2O(g)所具有的总能量大于CO2(g)与H2(g)所具有的总能量 |
| C、反应的热化学方程式是:CO(g)+H2O (g)=CO2 (g)+H2 (g);△H=+41kJ/mol |
| D、1mol CO2 (g)和1mol H2 (g)反应生成1molCO(g) 和1mol H2O(g)要放出41kJ热量 |
儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用.下列说法正确的是( )
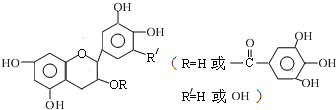

| A、常温下,儿茶素不溶于水,也不溶于有机溶剂 |
| B、儿茶素能与FeCl3溶液发生显色反应 |
| C、1mol儿茶素最多可与9mol NaOH反应 |
| D、儿茶素一定不能发生水解反应 |
a 克某物质在氧气中完全燃烧后的产物通过足量的Na2O2固体,固体质量增加a 克.此物质不可能的是( )
| A、CH3OH |
| B、CO和H2 |
| C、CO |
| D、CH4 |
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、含NA个Na+的Na2O2与1L水完全反应后所得溶液中Na+的物质的量浓度为1mol/L | ||
B、H2O通过Na2O2使其增重6 g时,反应中转移的电子数为
| ||
| C、6.2g氧化钠和7.8g过氧化钠的混合物中含有的离子总数为0.6NA | ||
| D、常温下,286 g Na2CO3?10H2O晶体中含有的CO32-小于NA个 |
下列混合物,能用分液漏斗进行分离的是( )
| A、水与酒精 | B、水与醋酸 |
| C、水与植物油 | D、水与蔗糖 |
工业上以铬铁矿(主要成分为FeO?Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7?2H2O),其主要反应为(1)4(FeO?Cr2O3)+8Na2CO3+7O2
8Na2CrO4+2Fe2O3+8CO2(2)2Na2CrO4+H2SO4═Na2SO4+Na2Cr2O7+H2O下列说法正确的是( )
| ||
| A、反应(1)和(2)均为氧化还原反应 |
| B、反应(1)中FeO?Cr2O3既是氧化剂又是还原剂 |
| C、高温下O2的氧化性大于Fe2O3小于Na2CrO4 |
| D、生成1mol的Na2Cr2O7时转移7mol电子 |
设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A、标准状况下,22.4L的氖气含约NA个氖原子 |
| B、常温常压下,1mol氨气中含有10 NA个电子 |
| C、标准状况下,22.4L水中含有3 NA个原子核 |
| D、0.3mol?L-1的K2SO4溶液中含有K+和SO42-总数为0.9NA |