题目内容
13.相同温度下,50mL0.01mol的CH3COOH溶液与5mL0.1mol的CH3COOH溶液相比较,下列数值前者大于后者的是( )| A. | 中和时所需KOH 的量 | B. | CH3COOH电离程度 | ||
| C. | H+的物质的量浓度 | D. | CH3COOH的物质的量 |
分析 50mL0.01mol的CH3COOH溶液与5mL0.1mol的CH3COOH溶液中含有醋酸的物质的量相等,
A.两溶液含有醋酸的物质的量相等,则中和时消耗氢氧化钾的物质的量相等;
B.醋酸浓度越大,电离程度越小;
C.醋酸溶液中,醋酸浓度越大,溶液中氢离子浓度越大;
D.两溶液中含有醋酸的物质的量相等.
解答 解:50mL0.01mol的CH3COOH溶液与5mL0.1mol的CH3COOH溶液中含有醋酸的物质的量都是0.0005mol,
A.两溶液中都含有0.0005mol醋酸,则中和时消耗KOH的物质的量相等,故A错误;
B.醋酸浓度越大,醋酸的电离程度越小,则电离程度前者大于后者,故B正确;
C.醋酸溶液中浓度越大,氢离子浓度越大,则氢离子浓度后者较大,故C错误;
D.两溶液中含有醋酸的物质的量相等,故D错误;
故选B.
点评 本题考查了弱电解质的电离平衡及其影响,题目难度不大,明确弱电解质溶液的浓度越大,其电离程度越小为解答关键,注意掌握电离平衡及其影响因素.

练习册系列答案
相关题目
3.下列有关概念说法正确的是( )
| A. | ${\;}_{1}^{1}$H+、${\;}_{1}^{2}$H2、${\;}_{1}^{3}$H是氢元素的三种同位素 | |
| B. | CH2═CH2和  属于同系物 属于同系物 | |
| C. | 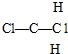 和 和 是甲烷的两种氯代物 是甲烷的两种氯代物 | |
| D. | 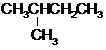 和 和 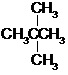 属于同分异构体 属于同分异构体 |
4.下列关于有机物的说法不正确的是( )
| A. | 甲烷可以发生取代不能发生加成 | |
| B. | 乙烯可以做水果催熟剂 | |
| C. | 甲烷和乙烯都可以使酸性高锰酸钾溶液褪色 | |
| D. | 乙烯可以加聚制备聚乙烯 |
1.目前,医疗上使用放射性核素$\stackrel{125}{53}$I治疗肿瘤,该核素原子核内的中子数是( )
| A. | 19 | B. | 53 | C. | 72 | D. | 125 |
8.有关晶体的下列说法中正确的是( )
| A. | 冰熔化时水分子中共价键发生断裂 | |
| B. | 原子晶体中共价键越强硬度越大 | |
| C. | 晶体中分子间作用力越大,分子越稳定 | |
| D. | 氯化钠溶于水时离子键未被破坏 |
18.一位德国化学家为苯分子结构的研究作出了巨大贡献,这位科学家是( )


| A. | 凯库勒 | B. | 道尔顿 | C. | 拉瓦锡 | D. | 门捷列夫 |
5.近年来,我国在超导材料研究方面居于世界领先地位,铊(Tl)是超导体的组成成分之一,铊位于第六周期第IIIA族.下列对铊的可能性质的推导正确的是( )
①原子半径比Al大 ②Tl(OH)3是两性氢氧化物
③Tl的阳离子氧化能力比Al的阳离子强 ④单质能与稀硝酸反应生成硝酸盐.
①原子半径比Al大 ②Tl(OH)3是两性氢氧化物
③Tl的阳离子氧化能力比Al的阳离子强 ④单质能与稀硝酸反应生成硝酸盐.
| A. | ①④ | B. | ②③ | C. | 只有① | D. | 只有④ |
2.某电池的总反应方程式为Pb+PbO2+4HBF4$?_{充电}^{放电}$2Pb(BF4)2+2H2,其中Pb(BF4)2、HBF4均是易溶于水的强电解质.下列说法中正确的是( )
| A. | 充电时,阳极附近溶液的pH增大 | |
| B. | 充电时,转移1 mol电子时阴极增加的质量为103.5 g | |
| C. | 放电时,BF4-向PbO2电极移动 | |
| D. | 放电时,正极的电极反应式为Pb+2e-+2H2O═Pb2++4OH- |
3.在标准状况下,等质量的CH4和CO2比较,下列说法中正确的是( )
| A. | 密度比4:1 | B. | 分子数之比为4:11 | ||
| C. | 体积比11:4 | D. | 物质的量之比为4:11 |