题目内容
4.短周期主族元素A、B、C、D,原子序数依次增大.A、C的原子序数的差为8,A、B、C三种元素原子的最外层电子数之和为10,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )| A. | 原子半径:A<B<C<D | |
| B. | 非金属性:A<C | |
| C. | 最高价氧化物对应水化物的酸性:D>C | |
| D. | B的最高价氧化物对应的水化物为强碱 |
分析 短周期主族元素A、B、C、D原子序数依次增大,B原子最外层电子数等于A原子最外层电子数的一半,则A原子最外层电子数为偶数,A、C的原子序数的差为8,则A、C为同主族元素,令B原子最外层电子数为x,则A、C的最外层电子数为2x,A、B、C三种元素原子的最外层电子数之和为10,则x+2x+2x=10,解的x=2,故A、C的最外层电子数为4,A为C元素,C为Si元素,B的原子序数大于C元素,最外层电子数为2,故B为Mg元素,D的原子序数大于Si,据此解答.
解答 解:短周期主族元素A、B、C、D原子序数依次增大,B原子最外层电子数等于A原子最外层电子数的一半,则A原子最外层电子数为偶数,A、C的原子序数的差为8,则A、C为同主族元素,令B原子最外层电子数为x,则A、C的最外层电子数为2x,A、B、C三种元素原子的最外层电子数之和为10,则x+2x+2x=10,解的x=2,故A、C的最外层电子数为4,A为C元素,C为Si元素,B的原子序数大于C元素,最外层电子数为2,故B为Mg元素,D的原子序数大于Mg,
A.同周期随原子序数增大原子半径减小,电子层越多原子半径越大,故原子半径B<A<D<C,故A错误;
B.同主族自上而下非金属性减弱,故非金属性C<A,故B错误;
C.非金属性D>C,故最高价氧化物对应水化物的酸性:D>C,故C正确;
D.B的最高价氧化物对应的水化物为氢氧化镁,为中强碱,故D错误,
故选:C.
点评 本题考查结构位置性质关系,难度中等,关键是利用奇偶性及A、C的原子序数相差8判断二者处于同一主族(短周期),注意短周期中原子序数相差8不一定为同主族,如H与F.

练习册系列答案
相关题目
15.已知A+、B2+、C-、D2-具有相同的电子层结构,有关A、B、C、D四种元素的叙述中正确的是( )
| A. | 原子序数:B>A>D>C | B. | 原子半径:A>B>C>D | ||
| C. | 金属性:A>B,非金属性:C>D | D. | 离子半径:D2->C->B2+>A+ |
12.在四个不同的容器中进行合成氨的反应.根据下列在相同时间内测定的结果,判断生成氨的速率最快的是( )
| A. | v(H2)=0.3 mol•L-1•min-1 | B. | v(N2)=0.05 mol•L-1•s-1 | ||
| C. | v(N2)=0.2 mol•L-1•min-1 | D. | v(NH3)=0.3 mol•L-1•min-1 |
9.碳及其化合物有广泛的用途.
(1)反应C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是BC.
A.增加碳的用量 B.升高温度
C.用CO吸收剂除去CO D.加入催化剂
(2)已知,C(s)+CO2(g)?2CO(g)△H=+172.5kJ•mol-1则反应
CO(g)+H2O(g)?CO2(g)+H2(g) 的△H=-41.2kJ•mol-1.
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
①其它条件不变,降低温度,达到新平衡前v(逆)<v(正)(填“>”、“<”或“=”).
②该温度下,此反应的平衡常数K=$\frac{9}{25}$;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数不变(填“增大”、“减小”或“不变”).
(1)反应C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,达到平衡后,体积不变时,以下有利于提高H2产率的措施是BC.
A.增加碳的用量 B.升高温度
C.用CO吸收剂除去CO D.加入催化剂
(2)已知,C(s)+CO2(g)?2CO(g)△H=+172.5kJ•mol-1则反应
CO(g)+H2O(g)?CO2(g)+H2(g) 的△H=-41.2kJ•mol-1.
(3)在一定温度下,将CO(g)和H2O(g)各0.16mol分别通入到体积为2.0L的恒容密闭容器中,发生以下反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下数据:
| t/min | 2 | 4 | 7 | 9 |
| n(H2O)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
②该温度下,此反应的平衡常数K=$\frac{9}{25}$;
③其它条件不变,再充入0.1mol CO和0.1mol H2O(g),达到平衡时CO的体积分数不变(填“增大”、“减小”或“不变”).
16.乙烷的二氯代物和四氯代物的种类相同,都为( )
| A. | 3种 | B. | 2种 | C. | 4种 | D. | 无法判断 |
10.以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:

(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在C的郊区(填标号)
A.有丰富黄铁矿资源的城市 B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市 D.人口稠密的文化、商业中心城市
(2)沸腾炉中发生反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$ 2Fe2O3+8SO2,接触室中发生反应的化学方程式是2SO2+O2$?_{△}^{催化剂}$ 2SO3.
(3)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是D.
A.硫铁矿燃烧前要粉碎,因为大块的黄铁矿不能在空气中反应
B.从沸腾炉出来的气体要净化,因为炉气中的SO2会与杂质反应
C.SO2氧化成SO3要用催化剂,这样可提高SO2的转化率
D.SO3用98.3%的浓硫酸来吸收,目的是为了防止形成酸雾,以提髙SO3吸收效率
(4)表是压强对SO2平衡转化率的影响
对于SO2转化SO3的反应,增大压强可使转化率升高,但在实际工业生产中常采用常压条件,理由是常压下转化率已经很高,增加压强可提高转化率,但增加了设备、动力成本等,效益反而下降.
(5)某工厂用500t含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是376.32tt.

(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在C的郊区(填标号)
A.有丰富黄铁矿资源的城市 B.风光秀丽的旅游城市
C.消耗硫酸甚多的工业城市 D.人口稠密的文化、商业中心城市
(2)沸腾炉中发生反应的化学方程式为4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$ 2Fe2O3+8SO2,接触室中发生反应的化学方程式是2SO2+O2$?_{△}^{催化剂}$ 2SO3.
(3)在硫酸工业制法中,下列生产操作与说明生产操作的主要原因二者都正确的是D.
A.硫铁矿燃烧前要粉碎,因为大块的黄铁矿不能在空气中反应
B.从沸腾炉出来的气体要净化,因为炉气中的SO2会与杂质反应
C.SO2氧化成SO3要用催化剂,这样可提高SO2的转化率
D.SO3用98.3%的浓硫酸来吸收,目的是为了防止形成酸雾,以提髙SO3吸收效率
(4)表是压强对SO2平衡转化率的影响
| 压强Mpa 转化率% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
(5)某工厂用500t含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是376.32tt.
11.不能使酸性KMnO4溶液褪色的是( )
| A. | 甲苯 | B. | 聚乙烯 | C. | SO2 | D. | 乙炔 |
 ,系统命名法命名为2,2,4,4-四甲基戊烷
,系统命名法命名为2,2,4,4-四甲基戊烷 ,系统命名法命名为2,2,3,3-四甲基戊烷
,系统命名法命名为2,2,3,3-四甲基戊烷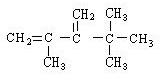 .
.