题目内容
15.下列图象正确的是( )| A. | 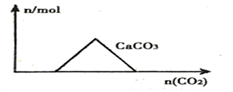 向Ca(OH)2和NaOH的混合溶液中通入CO2 | |
| B. | 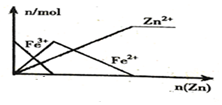 向FeCl3溶液中加入锌粉 | |
| C. | 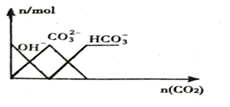 向NaOH溶液中通入CO2 | |
| D. | 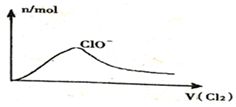 Cl2通入NaOH溶液中 |
分析 A.向Ca(OH)2和NaOH的混合溶液中通入CO2,CO2先与Ca(OH)2反应;
B.向FeCl3溶液中加入锌粉,先生成亚铁离子,亚铁离子再与Zn反应生成Fe;
C.向NaOH溶液中通入CO2,先生成碳酸钠,后来生成碳酸氢钠;
D.Cl2通入NaOH溶液中,生成NaCl和NaClO.
解答 解:A.向Ca(OH)2和NaOH的混合溶液中通入CO2,CO2先与Ca(OH)2反应,所以一开始就有碳酸钙沉淀生成,当Ca(OH)2全部反应后,再与NaOH反应,图象不符,故A错误;
B.向FeCl3溶液中加入锌粉,先生成亚铁离子,则铁离子的浓度减小,亚铁离子浓度增大,然后亚铁离子再与Zn反应生成Fe,亚铁离子浓度又减小,锌离子浓度一直增大,后来保持不变,图象符合,故B正确;
C.向NaOH溶液中通入CO2,先生成碳酸钠,碳酸根离子浓度增大,氢氧根离子浓度减小,当nmol氢氧根离子完全反应生成0.5nmol碳酸根离子,继续通入二氧化碳,碳酸根离子转化为碳酸氢根离子,最后生成nmol碳酸氢根离子,图象不符,故C错误;
D.Cl2通入NaOH溶液中,生成NaCl和NaClO,次氯酸根离子的浓度逐渐增大,当氢氧化钠完全反应时达到最大值,次氯酸根离子的浓度不会先增大后减小,故D错误.
故选B.
点评 本题考查了元素化合物的性质以及化学图象的有关内容,注意把握物质混合时发生的反应以及先后顺序为解题的关键,侧重于考查学生的分析能力和应用能力,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5.下列反应中,属于氧化还原反应的是( )
| A. | CaO+2HCl=CaCl2+H2O | B. | CaO+H2O=Ca(OH)2 | ||
| C. | CaCO3=CaO+CO2↑ | D. | 2 H2O2=2H2O+O2↑ |
6.镁-次氯酸盐燃料电池的工作原理如图所示,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-,下列有关说法正确的是( )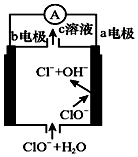

| A. | 电池工作时,c溶液中的溶质一定是MgCl2 | |
| B. | 负极反应式:ClO--2e-+H2O=Cl-+2OH- | |
| C. | 电池工作时,OH-向b电极移动 | |
| D. | b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl- |
3.下列叙述不正确的是( )
| A. | 在镀件上电镀铜时,可用金属铜作阳极 | |
| B. | 镀层破损后,白铁(镀锌)比马口铁(镀锡)更易被腐蚀 | |
| C. | 工业上电解饱和食盐水制烧碱,NaOH在阴极产生 | |
| D. | 钢铁在发生析氢腐蚀和吸氧腐蚀时,完全相同的反应是负极反应 |
10.在某恒温恒容密闭容器中,发生反应:A(g)+B(g)?2C(g)△H=-QkJ/mol,保持其它条件不变,只改变起始加入量,测得相关数据如表所示:下列说法中错误的是( )
| 起始加入量(mol) | 平衡时 | ||||
| A | B | C | A或C转化率(%) | C的物质的量分数(%) | 放出或吸收热量(KJ) |
| 1 | 1 | 0 | α1 | φ1 | Q1 |
| 0 | 0 | 2 | α2 | φ2 | Q2 |
| 2 | 2 | 0 | α2 | φ3 | Q3 |
| A. | α1+α2=1;φ2=φ1 | B. | φ3=2φ1;Q3=2Q1 | C. | φ3=φ1=φ2;Q3=2Q1 | D. | α1=α3;Q1+Q2=Q |
4.把6.4g Na2CO3和NaHCO3组成的固体混合物溶于水配成50mL溶液,其中c(Na+)=1.6mol•L-1.若把等质量的固体混合物加热至恒重,残留固体的质量是( )
| A. | 2.12 g | B. | 4.24 g | C. | 3.18 g | D. | 5.28 g |
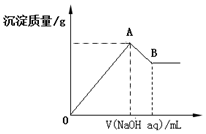 在含有0.60molCl-、0.80molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.
在含有0.60molCl-、0.80molSO42-及一定量Mg2+和Al3+的混合溶液中,滴入一定浓度NaOH溶液,产生沉淀情况如图(不考虑Mg2+和Al3+水解及水电离对离子数目的影响).若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x.