题目内容
(14分)认真观察下列装置,回答下列问题:

(1)装置B中PbO2上发生的电极反应方程式为________________________________。连接装置B、C的盐桥U形管中通常装填有 。
(2)装置A中总反应的离子方程式为 。装置D中NaCl溶液的pH会 (填“增大”、“不变”或“减小”)。
(3)若装置E的目的是在Cu材料上镀银,则X为__________,极板N的材料为________。若装置E的目的是防止某紫红色金属发生腐蚀,则极板N的材料为 。
(1)PbO2+4H++SO +2e-===PbSO4+2H2O 含有KCl溶液的琼脂
+2e-===PbSO4+2H2O 含有KCl溶液的琼脂
(2)Cu+2H+ Cu2++H2↑ 增大 (3)AgNO3 Ag 惰性电极(或石墨等不溶性惰性材料)
Cu2++H2↑ 增大 (3)AgNO3 Ag 惰性电极(或石墨等不溶性惰性材料)
【解析】
试题分析:(1)B和C装置形成原电池,铅作负极,二氧化铅作正极,原电池放电时,正极上二氧化铅得电子和硫酸根离子反应生成硫酸铅,发生还原反应,电极反应式为:PbO2+2e-+4H++SO42-=PbSO4+2H2O,盐桥一般用含有KCl溶液的琼脂;
(2)A为电解装置,铜为阳极,阴极生成氢气,电解方程式为Cu+2H+ Cu2++H2↑,D为电解饱和食盐水,生成氢氧化钠,溶液pH增大;
Cu2++H2↑,D为电解饱和食盐水,生成氢氧化钠,溶液pH增大;
(3)电镀时,镀层作阳极,镀件作阴极,电解质溶液中阳离子和镀层金属相同,若装置D的目的是在某镀件上镀银,则X为硝酸银溶液,N作阳极,应该是银,若装置E的目的是验证金属的电化学防腐,则极板N的材料为惰性电极(或石墨等不溶性惰性材料),被保护的金属连接电源阴极。
考点:考查原电池和电解池原理

 )的残留固体,若a点固体组成表示为PbOX或mPbO2·nPbO,列式计算x值和m:n值_ 。
)的残留固体,若a点固体组成表示为PbOX或mPbO2·nPbO,列式计算x值和m:n值_ 。

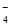 +6H++5H2O2===2Mn2++5O2↑+8H2O
+6H++5H2O2===2Mn2++5O2↑+8H2O
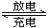 LixV2O5。下列说法中正确的是
LixV2O5。下列说法中正确的是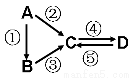
 KClO3 + 5KCl + 3H2O反应,以下说法错误的是
KClO3 + 5KCl + 3H2O反应,以下说法错误的是